题目内容
11.将 200g硝酸钾溶液分成质量相等两份,其中一份加入8g硝酸钾,另一份蒸发掉25g水,都恰好形成15℃时的饱和溶液,则15℃时硝酸钾的溶解度是32 g,原溶液中硝酸钾的质量分数为18.2%.分析 将100克硝酸钾溶液分成两等份,两份溶液完全相同,可把分别对两份溶液的处理看做是对同一份溶液的处理,得出5克溶质和20克水恰好形成饱和溶液的结论,再根据公式$\frac{溶质质量}{溶剂质量}=\frac{溶解度}{100g}$,求出溶解度;根据处理后的其中一份溶液中溶质的质量进一步求处理前的溶质质量,最后求质量分数.
解答 解:将 200g硝酸钾溶液分成质量相等两份,其中一份加入8g硝酸钾,另一份蒸发掉25g水,都恰好形成15℃时的饱和溶液,由于两份溶液完全相同,可把分别对两份溶液的处理看做是对同一份溶液的处理,故8克溶质和25克水恰好形成15℃时的饱和溶液,15℃时硝酸钾的溶解度为x,则$\frac{8g}{25g}=\frac{x}{100g}$,解得x=32g克;一份蒸发掉25克水后的溶液中的溶质质量为($\frac{200g}{2}-25g$)×$\frac{32g}{100g+32g}×100%$=18.2g,原溶液中硝酸钾的质量分数为$\frac{18.2g}{100g}×100%$=18.2%.
故答案为:32;18.2%.
点评 固体溶解度是初中化学的难重点,也是考查的重要热点,除考查对定义的理解,还涉及一些计算,正确理解溶解度的概念是解题的关键.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
13.下列四个短语,其原意一定包含化学变化的是( )
| A. | 花香四溢 | B. | 积土成山 | C. | 百炼成钢 | D. | 木已成舟 |
2.下列物质的用途仅与其物理性质有关的是( )
| A. | 用金刚石切割玻璃 | B. | 用氢气作高能燃料 | ||
| C. | 用生石灰作干燥剂 | D. | 用二氧化碳灭火 |
19.下列4个坐标图分别示意实验过程中某些量的变化,其中正确的是( )
| A | B | C | D |
| 向盛有MnO2的烧杯中加入H2O2溶液 | 在某一密闭装置内点燃红磷 | 加热一定量氯酸钾和二氧化锰固体混合物 | 向一定量石灰石中滴加稀盐酸 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
16.下列化学符号中的数字表示的意义不正确的是( )
| A. | SO2:“2”表示一个二氧化硫分子含有两个氧原子 | |
| B. | Mg+2:“+2”表示镁元素的化合价为+2价 | |
| C. | 2Na:“2”表示两个钠元素 | |
| D. | 2Cl-:“2”表示两个氯离子 |
3.物质的用途与性质密切相关.下列说法不正确的是( )
| A. | 古代画家用墨绘制的字画能保存很长时间而不变色,是因为碳化学性质不活泼 | |
| B. | 活性炭可用于制糖工业,是因为它具有吸附性 | |
| C. | 自来水煮沸可以降低硬度,是因为加热时水中的部分钙、镁离子形成了沉淀 | |
| D. | 铁制品表面涂“银粉”(即铝粉)防锈,是由于铝的化学性质比铁稳定 |
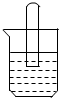 如图,将一个充满二氧化碳的试管倒立在盛有紫色石蕊溶液的烧杯中.
如图,将一个充满二氧化碳的试管倒立在盛有紫色石蕊溶液的烧杯中.