题目内容
某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其他杂质不与盐酸反应)。试计算:
(1)用10克30%的浓盐酸配制成2%的稀盐酸,需加水多少克?
(2)取20克废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸7.3克,求废水中氢氧化钾的质量分数。
第(1)题,用10克30%的浓盐酸配制成2%的稀盐酸需要向溶液中加入水,加水的过程中,溶质的质量是不变的。可根据这一点来计算。第(2)题7.3克盐酸中氯化氢的质量为7.3 g×2%,根据化学方程式可以求出反应物氢氧化钾的质量。然后用氢氧化钾的质量比上20 g废水便得废水中氢氧化钾的质量分数。
答案:解:(1)配制2%的稀盐酸的质量为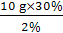 =150 g
=150 g
加入水的质量为150 g-10 g=140 g
(2)设参加反应的氢氧化钾的质量为x
HCl + KOH====KCl+H2O
36.5 56
7.3 g×2% x
36.5∶56=(7.3g×2%)∶x x=0.224 g
废水中氢氧化钾的质量分数为
 ×100%=1.12%
×100%=1.12%
答:略

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案请根据下表回答有关问题,除(2)题外其余各小题均用序号填空。
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
(1)表中的物质属于氧化物的 是 ;属于碱的是 ;属于盐的是 。
是 ;属于碱的是 ;属于盐的是 。
(2)利用表中的物质作为反应物,写出符合下列要求的化学方程式。
①有氧气生成的分解反应 ___________;
②有氢氧化钠生成的复分解反应 _________。
(3)若要测定纯碱溶液的酸碱度,可选用下列选项中的 。
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
(4)槟榔芋皮上含有一种碱性的物质——皂角素,皮肤沾上它会奇痒难忍。你认为可选用下列 来涂抹止痒。
①食醋(含醋酸) ②熟石灰 ③纯碱
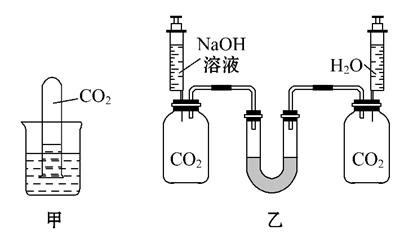
 变化情况。请问:
变化情况。请问: B.NO2 C.N2O5 D.NO
B.NO2 C.N2O5 D.NO B.厨房中的煤气大量泄漏时,应立即关闭气阀,不能打开抽油烟机排气
B.厨房中的煤气大量泄漏时,应立即关闭气阀,不能打开抽油烟机排气