题目内容
1.空气是人类活动必须的自然资源,工业常用分离液态空气的方法制取氧气,实验室常用物质分解的方法制取氧气.
(1)工业上制取氧气是物理(填“物理”或“化学”)变化.
(2)图中仪器a的名称是铁架台,b的名称是锥形瓶.
(3)实验室用一种液体原料来制取氧气,可选择B装置(填字母代号),此法制取氧气的化学反应方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)B装置的优点是能够控制反应速率.
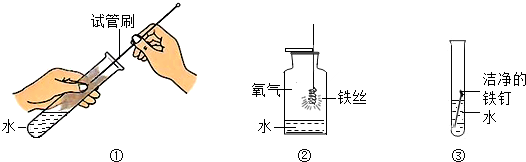
(5)如果用高锰酸钾制取氧气,则A装置需要改进的地方是在试管口放一团棉花.
分析 (1)根据工业利用液氧和液氮的沸点不同,常用分离液态空气的方法制取氧气解答;
(2)根据实验室常用仪器解答;
(3)根据实验室用双氧水和二氧化锰制取氧气是固液常温型的进行解答;
(4)根据装置特点分析解答;
(5)根据用高锰酸钾制取氧气的注意事项解答.
解答 解:
(1)工业利用液氧和液氮的沸点不同,常用分离液态空气的方法制取氧气,没有新物质生成,属于物理变化;
(2)根据实验室常用仪器可知:a是铁架台;b是锥形瓶;
(3)实验室用双氧水和二氧化锰制取氧气是固液常温型的,所以选择B,化学方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)B装置的优点是便于添加液体,能够控制反应速率;
(5)用高锰酸钾制取氧气,为防止高锰酸钾随气流进入导气管,则A装置需要改进的地方是在试管口放一团棉花;
答案:
(1)物理
(2)铁架台 锥形瓶
(3)B 2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(4)能够控制反应速率
(5)在试管口放一团棉花
点评 题尽管考查的知识内容不难,但由于考查的方式由整体选择变成化整为零地组合,需要对实验十分熟悉,没有经验是做不好的,一定要把原理搞懂,需要打破常规思维.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.沐川县城南新修的醉氧公园是集休闲度假、生态养生、文化体验于一体的城市公园.下列做法可能会增加公园空气中PM2.5的是( )
| A. | 为行走主干道洒水保洁 | B. | 在彩虹桥摄影留念 | ||
| C. | 举行老年人门球赛 | D. | 就地焚烧废纸、汽水瓶等垃圾 |
12.下列有关溶液的叙述正确的是( )
| A. | 稀溶液一定是不饱和溶液 | |
| B. | 饱和溶液就是不能再溶解任何物质的溶液 | |
| C. | 析出晶体后的溶液一定是饱和溶液 | |
| D. | 升温可使硝酸钾的不饱和溶液变为饱和溶液 |
9.下列物质的用途主要体现物质的物理性质的是( )
| A. |  用纯碱洗涤餐具 | B. |  用石墨作电刷 | ||
| C. |  在食品袋内充氮气防腐 | D. |  用干粉灭火器灭火 |
16.出Mg、Fe、Zn组成的混合物共40g,将其放入一定量的、质量分数为25%的稀硫酸溶液中,恰好完全反应将所得溶液蒸干,共得到固体136g,则在此过程中产生氧气质量为( )
| A. | 1g | B. | 4g | C. | 3g | D. | 2g |
6.某同学用氢氧化钙溶液和稀盐酸进行中和反应的实验时,忘记滴加指示剂,
于是他们决定对烧杯内溶液中的溶质成分进行探究.
(1)[做出猜想]
猜想一:可能是CaCl2和Ca(OH)2; 猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl.
(2)[实验探究]
(3)请写出一个上述实验过程中反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O,或Na2CO3+2HCl=2NaCl+H2O+CO2↑,或Na2CO3+CaCl2═CaCO3↓+2NaCl.
于是他们决定对烧杯内溶液中的溶质成分进行探究.
(1)[做出猜想]
猜想一:可能是CaCl2和Ca(OH)2; 猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl.
(2)[实验探究]
| 实验操作 | 实验现象 | 结论 |
| 取少量溶液,滴入酚酞溶液,振荡. | ①酚酞溶液不变色 | 猜想一不正确 |
| 另取少量溶液逐滴加入Na2CO3溶液至过量 | ②先产生气泡 后产生白色沉淀 | 猜想二不正确 猜想三正确 |
13.下列现象的描述中,正确的是( )
| A. | 打开盛浓盐酸的试剂瓶,观察到瓶口有白色烟雾产生 | |
| B. | 紫色石蕊溶液加入石灰水中,观察到溶液变为红色 | |
| C. | 在氢氧化钠溶液中滴加硫酸铜溶液,观察到产生蓝色沉淀 | |
| D. | 把一根洁净的铁钉加入稀硫酸中,观察到有气泡产生,溶液变为黄色 |