题目内容
19.学校化学试验室有一批锈迹斑斑的铁架台,同学们在老师的指导下进行翻新处理.(1)首先要除去表面的锈,有些同学用简单的物理方法除锈,方法为砂纸打磨.
(2)有些同学则用稀盐酸浸泡,开始观察到的现象为铁锈逐渐消失,无色溶液变成黄色,其中反应方程式为Fe2O3+6HCl═2FeCl3+3H2O.
(3)除锈后用清水冲洗干净,晾干,还需采取的防锈措施为喷漆.
分析 (1)用砂纸打磨可以除锈;
(2)铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁与水,写出反应的现象、化学方程式即可;
(3)防止金属生锈的方法通常是把金属和空气或水隔绝.
解答 解:(1)砂纸打磨可以除锈;
(2)铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入稀盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应现象为:铁锈逐渐消失,无色溶液变成黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
(3)铁架台防锈可以喷漆(或刷油漆),
故答案为:(1)砂纸打磨(2)铁锈逐渐消失,无色溶液变成黄色;Fe2O3+6HCl═2FeCl3+3H2O;(3)喷漆(或刷油漆).
点评 本题难度不大,掌握铁锈的主要成分、酸的化学性质、化学方程式的书写、防锈的方法等是正确解答本题的关键.

练习册系列答案
相关题目
10.下列不属于缓慢氧化的是( )
| A. | 动植物的呼吸 | B. | 钢铁生锈 | C. | 煤的燃烧 | D. | 酒和醋的酿造 |
7.下列物质的俗名与其化学式、物质分类相一致的是( )
| A. | 纯碱 Na2CO3 碱 | B. | 石灰石 CaCO3 盐 | ||
| C. | 生石灰 CaO 氧化物 | D. | 胆 矾 CuSO4盐 |
14.下列两种物质间能发生复分解反应的是( )
| A. | KNO3和NaCl | B. | Mg(OH)2和CuSO4 | C. | BaCO3和Na2SO4 | D. | NaOH和FeCl3 |
4.实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气.
(1)查阅资料:20℃时不同质量分数硫酸的密度(g/mL)如下表
分析以上数据,可以得出结论(任写1条)硫酸溶液中溶质的质量分数越大,溶液的密度越大(或硫酸溶液的密度比纯水的密度大);.
(2)计算:配制200g24.5%的稀硫酸,需98%浓硫酸多少毫升?请列式:V==$\frac{200g×24.5%}{98%×1.84g/mL}$(只列式不要求计算)
(3)配制稀硫酸:分别用量筒量取所需水和浓硫酸,先将水倒入烧杯中,再将浓硫酸沿着烧杯壁缓缓倒入,并用玻璃棒不断搅拌.
(1)查阅资料:20℃时不同质量分数硫酸的密度(g/mL)如下表
| 质量分数 | 4% | 10% | 16% | 24% | 32% | 36% | 44% | 49% | 60% | 98% |
| 密度 | 1.02 | 1.07 | 1.11 | 1.17 | 1.24 | 1.27 | 1.34 | 1.39 | 1.50 | 1.84 |
(2)计算:配制200g24.5%的稀硫酸,需98%浓硫酸多少毫升?请列式:V==$\frac{200g×24.5%}{98%×1.84g/mL}$(只列式不要求计算)
(3)配制稀硫酸:分别用量筒量取所需水和浓硫酸,先将水倒入烧杯中,再将浓硫酸沿着烧杯壁缓缓倒入,并用玻璃棒不断搅拌.
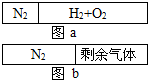 在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的四分之一处(图a),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图b),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )
在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的四分之一处(图a),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图b),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )