题目内容
5.化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1≠2”的事实是( )| A. | 20℃,1L水与1L酒精混合后的体积等于2L | |
| B. | 20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 | |
| C. | 20℃,1g镁和1g稀硫酸充分反应后所得的溶液质量为2g | |
| D. | 20℃,1g硝酸钾饱和溶液中加入1g硝酸钾固体能得到2g硝酸钾溶液 |
分析 A、分子之间有间隙,混合后,体积小于2L.
B、1g硫粉与1g氧气完全反应,根据质量守恒定律生成了2g二氧化硫.
C、1g镁和1g硫酸并没有完全反应,即使完全反应,由于氢气的外逸质量也不会等于2g.
D、硝酸钾的饱和溶液不会再溶解硝酸钾.
解答 解:A、分子之间有间隙,1L水与1L酒精混合后的体积小于2L,故A错误.
B、根据质量守恒定律,1g硫粉与1g氧气会完全反应,生成2g二氧化硫,故B正确.
C、1g镁和1g1g稀硫酸并没有完全反应,即使完全反应,由于氢气的外逸质量也不会等于2g,故C错误.
D、硝酸钾的饱和溶液不会再溶解硝酸钾,故不能得到2g硝酸钾溶液,故D错误.
故选B.
点评 本题主要考查学生运用质量守恒定律解答问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.某化学兴趣小组的同学按如图操作完成粗盐(含有难溶性杂质)提纯实验.下列说法正确的是( )

| A. | ④操作中待溶剂全部蒸干后再停止加热 | |
| B. | 正确的操作顺序为①⑤②③⑥④ | |
| C. | 去除难溶性杂质的步骤是④ | |
| D. | 操作③④中玻璃棒的作用是相同的 |
13.如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )


| A. | t1℃时,30g甲物质溶于70g水中得到30%的甲溶液 | |
| B. | t3℃时将甲、乙两物质的饱和溶液降温到t2℃,析出晶体质量甲>乙 | |
| C. | t2℃时,甲、丙溶液中溶质的质量分数甲>丙 | |
| D. | 将t3℃时甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液溶质的质量分数关系是乙>甲>丙 |
10.目前使用的燃料大多来自化石燃料.
(1)写出天然气中甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)分析下表,与煤相比,用天然气作燃料的优点有等质量的天然气和煤完全燃烧,天然气燃烧产生二氧化碳的质量少于煤,放出的热量多于煤.
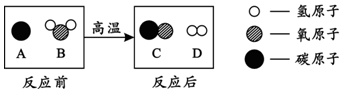
(3)为提高煤的利用率,可将其转化为可燃性气体,该反应的微观示意图如下,则生成物的分子个数比为1:1.
(1)写出天然气中甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)分析下表,与煤相比,用天然气作燃料的优点有等质量的天然气和煤完全燃烧,天然气燃烧产生二氧化碳的质量少于煤,放出的热量多于煤.
| 1g物质完全燃烧 | ||
| 产生二氧化碳的质量/g | 放出的热量/kJ | |
| 甲烷 | 2.75 | 56 |
| 煤碳 | 3.67 | 32 |

17.下列仪器的名称不正确的是( )
| A. |  酒精灯 | B. |  量筒 | C. |  试管 | D. |  长颈漏斗 |
14.如图是甲、乙、丙三种物质的溶解度曲线,下列分析不正确的是( )


| A. | t2℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是甲>乙>丙 | |
| B. | t2℃时,将50g甲物质放入100g水中充分溶解得到甲的饱和溶液 | |
| C. | 将t2℃时,三种物质的饱和溶液降温 至t1℃,所得溶液的溶质质量分数关 系是乙>甲=丙 | |
| D. | 将丙的饱和溶液变为不饱和溶液,可采用降温的方法 |
15.除去二氧化碳气体中混有的少量的一氧化碳,最合理的方法是( )
| A. | 点燃混合气体 | B. | 把混合气体通过氢氧化钠溶液中 | ||
| C. | 使混合气体通过灼热的氧化铜 | D. | 使混合气体通过灼热的焦炭 |

