题目内容
某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1 g二氧化锰混合,其总质量为6 g.依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
试计算:
(1)完全反应后产生的氧气的总质量为________.
(2)样品中氯酸钾的纯度是多少?
答案:
解析:
解析:
解:加热至t3、t4时间后剩余固体的质量不变,说明反应完全.
(1)根据质量守恒定律,产生氧气的质量应为6 g-4.08 g=1.92 g
(2)答:完全反应后产生的氧气的总质量为1.92 g,样品中氯酸钾的纯度为98%.
设产生1.92 g氧气需氯酸钾的质量为x,由反应的化学方程式可得
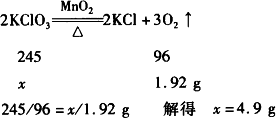
样品中氯酸钾的纯度为4.9 g/(6 g-1 g)×100%=98%

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物t1、t2、t3、t3时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
试计算:
(1)完全反应后产生的氧气的总质量为 .
(2)样品氯酸钾纯度是多少?
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 4.24 | 4.16 | 4.08 | 4.08 |
(1)完全反应后产生的氧气的总质量为
(2)样品氯酸钾纯度是多少?
某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物t1、、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
试计算:(1)完全反应后产生的氧气的总质量为 .
(2)样品中氯酸钾的纯度是多少?.
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 4.24 | 4.16 | 4.08 | 4.08 |
(2)样品中氯酸钾的纯度是多少?.