题目内容
19.实验室常用锌和稀硫酸反应来制取氢气.林辉同学取6.5g的锌片并加入50g溶质质量分数一定的稀硫酸,恰好完全反应,得到56.3g硫酸锌溶液.请计算:(1)生成氢气0.2g;
(2)稀硫酸中溶质的质量分数;
(3)反应后所得溶液中溶质质量分数是多少?
分析 锌和稀硫酸反应来制取氢气,同时生成硫酸锌;由参加反应的锌的质量,由反应的化学方程式列式计算出生成氢气的质量、稀硫酸中溶质的质量、生成硫酸锌的质量,进而计算出稀硫酸中溶质的质量分数、反应后所得溶液中溶质质量分数.
解答 解:设生成氢气的质量为x,稀硫酸中溶质的质量为y,生成硫酸锌的质量为z,
Zn+H2SO4═ZnSO4+H2↑
65 98 161 2
6.5g y z x
(1)$\frac{65}{2}=\frac{6.5g}{x}$ x=0.2g.
(2)$\frac{65}{98}=\frac{6.5g}{y}$ y=9.8g
稀硫酸中溶质的质量分数为$\frac{9.8g}{50g}$×100%=19.6%.
(3)$\frac{161}{65}=\frac{z}{6.5g}$ z=16.1g
反应后所得溶液中溶质质量分数是$\frac{16.1g}{6.5g+50g-0.2g}$×100%≈28.6%.
答:(1)0.2;(2)稀硫酸中溶质的质量分数为19.6%;(3)反应后所得溶液中溶质质量分数是28.6%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.亮亮做家务时接触到下列用品.
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是Fe与潮湿的空气接触.
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
| 用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
7.下列关于物质的性质和用途说法正错误的是( )
| A. | 石墨有滑腻感,可以做电极 | |
| B. | 氮气化学性质不活泼,可用于食品防腐 | |
| C. | 活性炭有吸附性,可吸附异味 | |
| D. | 金刚石的硬度大,可切割玻璃 |
14.依据如图进行实验(夹持仪器略去).实验过程:①通入N2,点燃酒精灯,一段时间后,a、b中均无明显现象;②熄灭酒精灯,立即改通O2,a中无明显现象,b中红磷燃烧,下列有关该实验的说法不正确的是( )
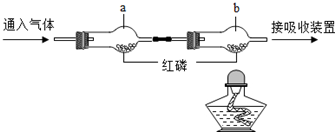

| A. | 实验过程①中,能说明N2不支持燃烧 | |
| B. | 实验过程①中,将氮气换为二氧化碳也能得出燃烧的有关条件 | |
| C. | 实验过程②中,红磷燃烧时产生大量白烟 | |
| D. | 实验过程②中,能说明可燃物燃烧的条件之一是与氧气接触 |
11.下列说法正确的是( )
| A. | 酸和碱的反应一定是中和反应 | |
| B. | 物质一定都由分子构成 | |
| C. | 含碳元素的物质燃烧一定生成二氧化碳 | |
| D. | 元素化学性质相似,原子最外层电子数一定相等 |