题目内容
20.甲、乙、丙、丁四位同学分别取某石灰样品于50g盐酸进行实验(杂质不与盐酸反应)所得实验数据见表:| 实验 | 甲 | 乙 | 丙 | 丁 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | 4.4 |
(2)该石灰石样品中碳酸钙的质量分数.
分析 (1)根据表中的数目对比分析50g盐酸完全反应后生成二氧化碳的总质量,根据二氧化碳的质量计算出氯化氢的质量,再除以50g盐酸质量即可;
(2)根据5g样品中与盐酸反应生成的二氧化碳的质量算出碳酸钙的质量,再除以样品的质量即可.
解答 【解答】解:(1)由表中的数据可知,50g盐酸完全反应完只能生成4.40g二氧化碳;
50g盐酸溶液中溶质的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
x 4.4g
$\frac{73}{44}=\frac{x}{4.4g}$ 解得:x=7.3g,
所以盐酸中溶质的质量分为:$\frac{7.3g}{50g}$×100%=14.6%.
(2)由表中的数据可知,5g样品中的碳酸钙与盐酸完全反应后生成二氧化碳的质量为1.76g.
设5g样品中的碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
y 1.76g
$\frac{100}{44}=\frac{y}{1.76g}$ 解得:y=4g
该石灰石样品中碳酸钙的质量分数是:$\frac{4g}{5g}×100%$=80%
故答案为:(1)14.6%;(2)该石灰石样品中碳酸钙的质量分数80%.
点评 解答本题关键是要知道根据图表中数据分析哪种物质过量的方法,计算样品中碳酸钙含量时,必须要根据样品完全反应的那次进行计算,计算盐酸质量分数时,要根据盐酸完全反应的那次进行计算.

练习册系列答案
相关题目
10.向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液,关于该滤渣和滤液有下列四种说法,正确的是( )
| A. | 向滤渣中加稀盐酸,一定有气泡产生 | |
| B. | 向滤液中加稀盐酸,可能有沉淀产生 | |
| C. | 滤渣中一定含Ag,可能含有Fe和Al | |
| D. | 滤液中一定含Fe(NO3)2,可能含Al(NO3)2 |
8.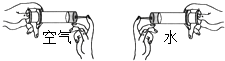 《运动的水分子》这节课上,老师让同学做了如图对照试验,其中所得结论不正确的是( )
《运动的水分子》这节课上,老师让同学做了如图对照试验,其中所得结论不正确的是( )
 《运动的水分子》这节课上,老师让同学做了如图对照试验,其中所得结论不正确的是( )
《运动的水分子》这节课上,老师让同学做了如图对照试验,其中所得结论不正确的是( )| A. | 水是由水分子构成的 | |
| B. | 空气是由空气分子构成的 | |
| C. | 装空气的注射器容易被压缩是因为气体分子间间隔较大 | |
| D. | 空气被压缩,水被压缩都属于物理变化 |
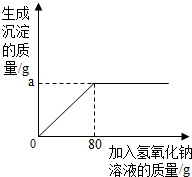 工业上用卤水(主要是MgCl2溶液,另外含少量NaCl)为原料,提纯得到氯化镁.再在熔融状态下电解氯化镁制取金属镁.卤水中氯化镁的含量,需通过实验测得,检验员取100g卤水,向里滴加20%的氢氧化钠溶液,所加氢氧化钠溶液质量与所得沉淀的质量关系 如图所示.
工业上用卤水(主要是MgCl2溶液,另外含少量NaCl)为原料,提纯得到氯化镁.再在熔融状态下电解氯化镁制取金属镁.卤水中氯化镁的含量,需通过实验测得,检验员取100g卤水,向里滴加20%的氢氧化钠溶液,所加氢氧化钠溶液质量与所得沉淀的质量关系 如图所示.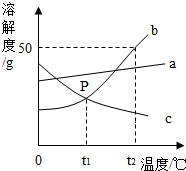 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题: