题目内容
2.利用如图实验装置测定某氧化铜样品中氧化铜的质量分数.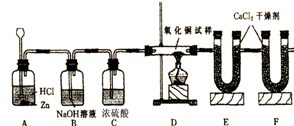
(1)装置B、C的作用分别是装置B吸收氯化氢气体,装置C吸收水蒸气
(2)假设样品中的杂质不反应,且B、C、E装置吸收均完全.取10克样品,若实验前称得U型管E和其中的氯化钙质量为100.8克,充分反应后称得U型管E总质量为102.6克,则样品中氧化铜的质量分数为80%.
(3)若取消F装置,那么测得的样品中氧化铜的质量分数比实际样品中氧化铜的质量分数偏大(填“偏大”或“偏小”).
分析 (1)根据氢氧化钠溶液能吸收氯化氢气体、浓硫酸能吸收水蒸气分析装置B、C的作用;
(2)根据氯化钙能吸收水的质量,求出氧化铜的质量,再求出样品中氧化铜的质量分数;
(3)根据空气中含有水蒸气分析.
解答 解:(1)由于氢氧化钠溶液能吸收氯化氢气体、浓硫酸能吸收水蒸气,所以装置B、C的作用分别是:装置B吸收氯化氢气体,装置C吸收水蒸气;
(2)生成水的质量:102.6g-100.8g=1.8g;
设氧化铜的质量为x
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O
80 18
x 1.8g
$\frac{80}{18}=\frac{x}{1.8g}$ 解得:x=8g,
样品中氧化铜的质量分数为:$\frac{8g}{10g}×100%$=80%
(3)由于空气中含有水蒸气,若取消F装置,那么测得的样品中氧化铜的质量分数比实际样品中氧化铜的质量分数偏大.
故答为:(1)装置B吸收氯化氢气体,装置C吸收水蒸气;(2)80%;(3)偏大.
点评 本题的难度不大,主要考查了常见物质的性质和根据化学方程式的简单计算,根据已有的知识分析解答即可.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
10.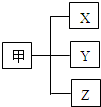 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )| 选项 | 甲 | X | Y | Z |
| A | 常见的碱 | 烧碱 | 纯碱 | 熟石灰 |
| B | 常见的有机物 | 甲烷 | 酒精 | 脂肪 |
| C | 常见的合金 | 铝合金 | 钢 | 氧化铁 |
| D | 常见的不溶性盐 | 硫酸钡 | 氯化银 | 氢氧化铁 |
| A. | A | B. | B | C. | C | D. | D |
11.除去下列物质中的少量杂质,所选用的试剂及操作方法正确的是( )
| 选项 | 物质(括号内为杂质) | 试 剂 | 操作方法 |
| A | CO2(CO) | 氧气 | 点燃 |
| B | Fe(CuSO4粉末) | H2O | 溶解后过滤、洗涤、干燥 |
| C | CuO(炭粉) | 足量氧气 | 充分加热 |
| D | MnO2(KClO3) | 充分加热后,冷却 |
| A. | A | B. | B | C. | C | D. | D |
12.下列有关分子和原子的说法中,正确的是( )
| A. | 原子是保持物质化学性质的最小粒子 | |
| B. | 保持水化学性质的粒子是氢原子和氧原子 | |
| C. | 分子的质量总是比原子的质量大 | |
| D. | 分子和原子都可以构成物质 |
 我们知道,空气的主要成分是氮气和氧气.如图是测空气中氧气含量的实验装置.试回答下列问题:
我们知道,空气的主要成分是氮气和氧气.如图是测空气中氧气含量的实验装置.试回答下列问题:

 不同类别的物质间存在着一定的关系,碳酸钠溶液、氢氧化钠溶液和稀盐酸之间的变化关系如图1所示(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质).则
不同类别的物质间存在着一定的关系,碳酸钠溶液、氢氧化钠溶液和稀盐酸之间的变化关系如图1所示(“-”表示相连的两种物质能发生反应,“→”表示某种物质可转化为另一种物质).则