题目内容
11.海水是一种重要的自然资源(海水中含NaCl、MgCl2等物质),被誉为“国防金属”的镁主要是从海水中提取的,下面是从海水中提取金属镁的简单流程.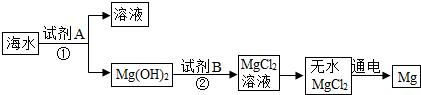
(1)试剂A的化学式为Ca(OH)2.
(2)操作①的名称是过滤.
(3)由无水MgCl2制取Mg的化学方程式为MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(4)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:通过步骤①、②得到的氯化镁溶液浓度远高于海水中氯化镁的浓度.
分析 氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙;
通电条件下,氯化镁分解生成镁和氯气.
解答 解:(1)试剂A是氢氧化钙,氢氧化钙的化学式为Ca(OH)2.
故填:Ca(OH)2.
(2)操作①的名称是过滤,通过过滤把液体和固体分离.
故填:过滤.
(3)通电条件下,氯化镁分解生成镁和氯气,反应的化学方程式为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
故填:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(4)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液的不同之处是:通过步骤①、②得到的氯化镁溶液浓度远高于海水中氯化镁的浓度.
故填:通过步骤①、②得到的氯化镁溶液浓度远高于海水中氯化镁的浓度.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
2.我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向饱和的食盐水中通入氨气,制成饱和铵盐水;②在加压条件下向饱和铵盐水中通入二氧化碳,两者发生反应生成碳酸氢钠,有晶体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水.四种盐在不同温度下的溶解度表:
请回答:(1)碳酸氢铵的化学式是NH4HCO3.
(2)由上表分析过程②中能发生反应的原因是在相同温度下碳酸氢钠的溶解度最小.
| 温度 溶解度/g 盐 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | ------- | ------- |
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 | ------- |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(2)由上表分析过程②中能发生反应的原因是在相同温度下碳酸氢钠的溶解度最小.
6.我市频临渤海,蕴藏丰富的海洋资源.下列对海洋化学资源利用的有关叙述错误的是( )
| A. | 利用多级闪急蒸馏法淡化海水 | |
| B. | 利用蒸发结晶的方法从海水中提取食盐 | |
| C. | 利用向海水或卤水中加入石灰乳的方法将海水中的Mg2+富集沉淀出来 | |
| D. | 利用海底蕴藏的大量“可燃冰”作燃料,以它为燃料不会加剧温室效应 |
1.人吸入的空气与呼出的气体相比,呼出的气体中明显增加的气体是( )
| A. | 氧气 | B. | 氧气和二氧化碳 | ||
| C. | 氮气 | D. | 二氧化碳和水蒸气 |