题目内容
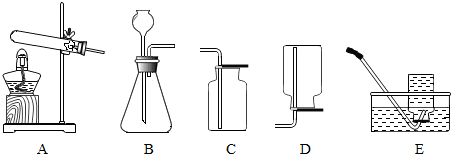
向一支装有少量CuO的试管中依次加入下列物质(每次加入物质均充分为),实验过程如下:

(1)从物质分类角度看,CuO属于 (填“酸”“碱”“盐”“氧化物”).
(2)图B实验中有蓝色沉淀生成,其反应的化学方程式为 .
(3)如图D,向图C实验后所得溶液中插入新打磨的铝丝:
①在铝丝表面能观察到的现象是 ;
②反应停止后,所得溶液中一定含有的溶质是 .

(1)从物质分类角度看,CuO属于
(2)图B实验中有蓝色沉淀生成,其反应的化学方程式为
(3)如图D,向图C实验后所得溶液中插入新打磨的铝丝:
①在铝丝表面能观察到的现象是
②反应停止后,所得溶液中一定含有的溶质是
考点:酸的化学性质,金属的化学性质,碱的化学性质,常见的氧化物、酸、碱和盐的判别,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料,常见的酸 酸的通性,常见的碱 碱的通性
分析:(1)根据物质的组成确定种类;
(2)根据反应物和产物书写化学方程式;
(3)依次根据反应情况对反应后溶液中的溶质进行分析,以便确定反应现象及溶液中的溶质.
(2)根据反应物和产物书写化学方程式;
(3)依次根据反应情况对反应后溶液中的溶质进行分析,以便确定反应现象及溶液中的溶质.
解答:解:(1)氧化铜是由氧元素和铜元素组成的氧化物;
(2)硫酸铜与氢氧化钠反应生成氢氧化铜沉淀的硫酸钠,化学方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
(3)A:过量的硫酸与氧化铜反应,反应后的溶液中含有硫酸铜和硫酸;B:将过量的氢氧化钠加入上述溶液中,分别与硫酸和硫酸铜反应,生成硫酸钠和氢氧化铜沉淀,故反应后的溶液中含有硫酸钠和剩余的氢氧化钠;C:将过量的硫酸加入上述溶液中,分别于氢氧化钠和氢氧化铜反应,生成硫酸钠和硫酸铜,故反应后的溶液中含有硫酸钠、硫酸铜和剩余的硫酸;D:向上述溶液中加入铝丝,会与硫酸铜和硫酸反应,生成金属铜、氢气和硫酸铝,故现象为铝丝表面有红色物质析出,有气泡冒出;反应停止后,所得溶液中一定含有的溶质是Al2(SO4)3;Na2SO4.
故答案为:(1)氧化物;
(2)CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
(3)铝丝表面有红色物质析出,有气泡冒出;
(4)Al2(SO4)3 Na2SO4
(2)硫酸铜与氢氧化钠反应生成氢氧化铜沉淀的硫酸钠,化学方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
(3)A:过量的硫酸与氧化铜反应,反应后的溶液中含有硫酸铜和硫酸;B:将过量的氢氧化钠加入上述溶液中,分别与硫酸和硫酸铜反应,生成硫酸钠和氢氧化铜沉淀,故反应后的溶液中含有硫酸钠和剩余的氢氧化钠;C:将过量的硫酸加入上述溶液中,分别于氢氧化钠和氢氧化铜反应,生成硫酸钠和硫酸铜,故反应后的溶液中含有硫酸钠、硫酸铜和剩余的硫酸;D:向上述溶液中加入铝丝,会与硫酸铜和硫酸反应,生成金属铜、氢气和硫酸铝,故现象为铝丝表面有红色物质析出,有气泡冒出;反应停止后,所得溶液中一定含有的溶质是Al2(SO4)3;Na2SO4.
故答案为:(1)氧化物;
(2)CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
(3)铝丝表面有红色物质析出,有气泡冒出;
(4)Al2(SO4)3 Na2SO4
点评:解决本题的关键是明确反应情况及反应后溶液中的溶质.

练习册系列答案
相关题目
 H7N9禽流感引起社会的高度关注.2013年4月5日,一种新型的抗流感新药帕拉米韦氯化钠注射液被国家食品药品监督管理总局加速批准上市.帕拉米韦的化学式为C15H28N4O4.下列对帕拉米韦的有关说法正确的是( )
H7N9禽流感引起社会的高度关注.2013年4月5日,一种新型的抗流感新药帕拉米韦氯化钠注射液被国家食品药品监督管理总局加速批准上市.帕拉米韦的化学式为C15H28N4O4.下列对帕拉米韦的有关说法正确的是( )| A、该物质是由多种原子构成的化合物 |
| B、该物质中含有28个氢原子 |
| C、该物质由碳、氢、氮、氧四种元素组成 |
| D、该物质中碳、氢元素的质量比为15:28 |