题目内容
6.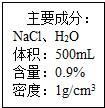 如图是一瓶医用注射盐水标签的部分内容.
如图是一瓶医用注射盐水标签的部分内容.(1)配制该瓶盐水需要氯化钠的质量多少克?
(2)若将该瓶盐水溶质的质量分数增大一倍,需要蒸发多少克水?
(3)若用4.5%的氯化钠溶液来配制该瓶盐水,需要4.5%的氯化钠溶液多少克?
分析 (1)根据溶质的质量分数计算公式进行计算分析解答.
(2)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答 解:(1)500mL=500cm3,配制该瓶盐水需要氯化钠的质量为:500cm3×1g/cm3×0.9%=4.5g;
(2)若将该瓶盐水溶质的质量分数增大一倍,设需要蒸发水的质量为x
$\frac{500c{m}^{3}×1g/c{m}^{3}×0.9%}{500c{m}^{3}×1g/c{m}^{3}-x}×100%$=0.9%×2 解得:x=250g;
(3)若用4.5%的氯化钠溶液来配制该瓶盐水,设需要4.5%的氯化钠溶液的质量为y
4.5%×y=4.5g 解得:y=100g
答:(1)配制该瓶盐水需要氯化钠的质量是4.5克;(2)需要蒸发250克水;(3)需要4.5%的氯化钠溶液100克.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用溶质质量分数的有关计算、溶液稀释前后溶质的质量不变进行分析问题、解决问题的能力.

练习册系列答案
相关题目
14.科学家在制备C60和碳纳米管时得到一种副产物.其外观类似泡沫、质地轻盈,由碳的微小颗粒组成,称为碳纳米泡沫,它的发现极大地推动了碳素材料的研究.下列说法错误的是( )
| A. | 碳纳米泡沫是一种化合物 | |
| B. | 碳纳米泡沫和碳纳米管属于不同种物质 | |
| C. | 碳纳米泡沫完全燃烧的产物是二氧化碳 | |
| D. | 碳纳米泡沫在一定条件下可以置换氧化铜 |
1.对下列实验过程的评价,正确的是( )
| A. | 某固体中加入稀盐酸,产生无色气体,证明该固体中一定含有CO32- | |
| B. | 某溶液中加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO42- | |
| C. | 某无色溶液滴入酚酞试液变红色,该溶液一定是碱溶液 | |
| D. | 验证烧碱溶液中是否含有Cl-,应先加硝酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含有Cl- |
11.已知某合金的金属粉末原料中可能含有铁、锌、铜三种金属中的两种成三种,化学小组的同学对该粉末进行探究.
(1)提出猜想:
猜想一:该粉末由铜、锌组成;
猜想二:该粉末由铁、锌组成;
猜想三:该粉末由铜、铁、锌组成;
(2)进行实验:
(3)初步结论:猜想三成立;实验①中发生反应的化学方程式Fe+H2SO4═FeSO4+H2↑(任写一个即可).
(1)提出猜想:
猜想一:该粉末由铜、锌组成;
猜想二:该粉末由铁、锌组成;
猜想三:该粉末由铜、铁、锌组成;
(2)进行实验:
| 实验目的 | 实验操作 | 实验现象 |
| ①证明粉末中是否含有铜 | 取一个小烧杯加入适量的粉末,再向其中加入足量的稀硫酸. | 有少量红色粉末不能溶解. |
| ②证明粉末中是否含有锌 | 取一定量粉末放于烧杯中,加入适量的FeSO4溶液,反应完全后过滤、干燥、称量、固体质量减少了 | 溶液由浅绿色变成了无色 |
| ③证明粉末中是否含有铁 | 另取一定量该粉末,用用磁铁充分吸引(用物理方法),称量剩余粉末减少了 | 有大量黑色粉末被磁铁吸引 |
18.下列说法中,错误的是( )
| A. | 有单质参加或有单质生成的反应不一定是置换反应 | |
| B. | 化学反应的发生伴随着能量的变化 | |
| C. | 水变成水蒸气发生的是物理变化,水分子本身未变,只是分子间的空隙变大 | |
| D. | 取A、B两种物质各10g混合,充分反应后生成物的总质量一定为20g |
15.下列有关空气及其成分的说法正确的是( )
| A. | 按质量计算,空气中含有氮气约78%,氧气约21% | |
| B. | 氧气在低温、加压的条件下可以转变为淡蓝色的液体或固体 | |
| C. | 氧气的化学性质比较活泼,是可燃物 | |
| D. | 因为氧气与氮气的密度不同,所以工业上用分离液态空气法制取氧气 |
16.如图所示实验操作正确的是( )
| A. |  加热液体 | B. | 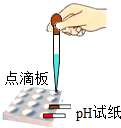 测定溶液pH | C. | 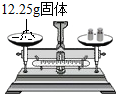 称量固体 | D. |  稀释浓硫酸 |