题目内容
14.用所学的化学原理或化学方程式解释下列现象.(1)用汽油洗去衣服上的油污的原理是汽油能溶解油污.
(2)可用适量的稀盐酸除去锅炉里的水垢[主要成分为CaCO3、Mg(OH)2],用化学方程式表示其反应之一:CaCO3+2HCl=CaCl2+H2O+CO2↑(或Mg(OH)2+2HCl=MgCl2+2H2O);稀盐酸选用适量而不是过量,是因为多余盐酸会与铁反应,导致铁锅受损..
(3)氢氧化钾是我国古代纺织业常用作漂洗的洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧后的固体(主要成分是氧化钙)与草木灰(主要成分是碳酸钾)在水中相互作用,就生成了氢氧化钾.请按要求用化学方程式表示上述反应:
①分解反应CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
②化合反应CaO+H2O=Ca(OH)2;
③复分解反应K2CO3+Ca(OH)2=CaCO3↓+2KOH.
分析 (1)根据用汽油洗去衣服上的油污的原理是汽油能溶解油污解答;
(2)根据反应物、生成物利用质量守恒定律,写出反应的方程式;根据稀盐酸选用适量而不是过量,是因为多余盐酸会与铁反应,导致铁锅受损解答;
(3)根据教材中学习的知识,碳酸钙灼烧时可以分解生成氧化钙和二氧化碳,而氧化钙遇水会化合生成氢氧化钙,氢氧化钙与碳酸钾发生复分解反应生成碳酸钙沉淀和氢氧化钾.
解答 解:
(1)用汽油洗去衣服上的油污的原理是汽油能溶解油污;
(2)稀盐酸和碳酸钙反应,生活才呢个氯化钙、水和二氧化碳气体,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;盐酸和氢氧化镁反应,生成氯化镁和水,化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O;稀盐酸选用适量而不是过量,是因为多余盐酸会与铁反应,导致铁锅受损;
(3)
①碳酸钙灼烧时可以分解生成氧化钙和二氧化碳,根据分解反应的定义可以知道,该反应属于分解反应,故答案为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
②氧化钙遇水会化合生成氢氧化钙,根据化合反应的定义可知,该反应属于化合反应,故答案为:CaO+H2O=Ca(OH)2
③氢氧化钙与碳酸钾发生复分解反应生成碳酸钙沉淀和氢氧化钾,故答案为:K2CO3+Ca(OH)2=CaCO3↓+2KOH
答案:
(1)汽油能溶解油污
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑(或Mg(OH)2+2HCl=MgCl2+2H2O)
多余盐酸会与铁反应,导致铁锅受损.
(3)
①CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑
②CaO+H2O=Ca(OH)2
③K2CO3+Ca(OH)2=CaCO3↓+2KOH
点评 此题联系生活生产实际,主要考查了三种常见的主要反应类型,是初中化学的重点内容,中考的考点之一.


| A. | 在化学反应中,硫原子容易失去电子 | |
| B. | 硫元素的核电荷数为16 | |
| C. | 硫元素的相对原子质量为32.06g | |
| D. | 硫氧气中燃烧产生明亮的淡蓝色火焰 |
(1)提出合理假设:
滤液中一定含有NaCl(填化学式,下同),滤液中除该物质外,溶质有4种可能:
猜想①BaCl2;猜想②:Na2SO4;猜想③:Na2CO3; 猜想④:Na2CO3、Na2SO4
(2)完成实验方案.请填写实验操作、与表中结论相符的预期现象.
(实验室仅提供下列试剂:稀硫酸、稀盐酸、氢氧化钡溶液)
| 实验操作 | 预期现象 | 结论 |
| 步骤1: 向滤液中加入足量的氢氧化钡溶液 | 产生白色沉淀 | 猜想④成立 |
| 步骤2: 过滤,向白色沉淀中加入足量的稀盐酸 | 沉淀部分溶解,产生气泡 |
| A. |  称取食盐 | B. |  稀释浓硫酸 | C. |  测定溶液的pH | D. |  固体药品的取用 |
| A. | 提倡焚烧秸秆 | |
| B. | 向煤炭中加入石灰石或生石灰作固硫剂,减少二氧化硫的排放 | |
| C. | 出行时步行或骑自行车,尽可能的少开私家车 | |
| D. | 禁止燃放烟花爆竹 |
| A. | 铁 | B. | 钙 | C. | 锌 | D. | 碘 |
| A. | 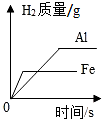 等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| B. |  表示水通电分解产生的气体质量与反应时间的关系 | |
| C. | 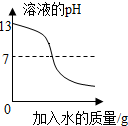 向pH=13的氢氧化钠溶液中不断加水稀释 | |
| D. |  化学反应中,原子总数随时间的变化 |