题目内容
15.某密闭容器中有X、氧气、二氧化碳三种物质,在一定条件下充分反应,反应前后各物质质量的数据记录如下:| 物质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 46 | 128 | 1 | 0 |
| 反应后的质量/g | 0 | 待测 | 89 | 54 |
| A. | 物质X由碳、氢元素组成 | B. | 物质X由碳、氢、氧元素组成 | ||
| C. | 充分反应后剩余氧气质量为16克 | D. | 生成CO2与H2O的质量比是89:54 |
分析 反应后X质量减少46g,是反应物;
反应后二氧化碳增加88g,是生成物;
反应后水增加54g,是生成物;
根据质量守恒定律可知,氧气是反应物,参加反应的氧气质量为:88g+54g-46g=96g,则待测为:128g-96g=32g.
解答 解:二氧化碳中的碳元素和水中的氢元素来自于X,88g二氧化碳中碳元素的质量为:88g×$\frac{12}{44}$×100%=24g;54g水中氢元素的质量为:54g×$\frac{2}{18}×100%$=6g,24g+6g=30g<46g,故X中一定含有氧元素;
A、物质X由碳、氢、氧元素组成,错误;
B、物质X由碳、氢、氧元素组成,正确;
C、充分反应后剩余氧气质量为32克,错误
D、生成CO2与H2O的质量比是88:54,错误
故选B.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
6.下列图象不能正确反映其变化过程的是( )
| A. |  镁在装有空气的密闭容器内燃烧 | |
| B. |  电解水生成气体的体积 | |
| C. |  浓硫酸长期露置在空气中 | |
| D. |  向空气中部分变质的氢氧化钠溶液中滴加稀盐酸 |
3.下列实验方案不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别棉线和羊毛线 | 灼烧,闻气味 |
| B | 鉴别氯化铵和硫酸钠 | 加熟石灰研磨,闻气味 |
| C | 除去二氧化碳中少量的一氧化碳 | 点燃混合气体 |
| D | 检验氯化钠固体中是否混有碳酸钠 | 加入适量稀盐酸,看是否有气泡产生 |
| A. | A | B. | B | C. | C | D. | D |
10.某品牌矿泉水的标签上标明的矿泉水主要成分如下表所示,请根据本表回答下列问题:
①碳酸氢钙的化学式是Ca(HCO3)2.
②二个镁离子的化学符号是2Mg2+.
③用结构示意图表示Cl-的核外电子排布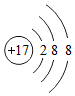 .
.
④请在偏硅酸化学式中标记硅元素的化合价H2$\stackrel{+4}{Si}$O3.
⑤矿泉水属于混合物(填“纯净物”或“混合物”).
⑥淡水资源有限,我们需要节约用水,如图中表示节水标志的是
| 水质主要成分(mg/L) | |
| 偏硅酸(H2SiO3) 28.9-42.9 碳酸氢根(HCO${\;}_{3}^{-}$) 173-205 氯离子(Cl-) 1.0-8.0 硫酸根(SO42-) 16.06-19.52 镁 2.5-7.5 | 锶(Sr) 0.01-0.32 钙 5-45 钠(Na+)45-70 钾(K+) 0.5-2.0 PH 7.8±0.5 |
②二个镁离子的化学符号是2Mg2+.
③用结构示意图表示Cl-的核外电子排布
 .
.④请在偏硅酸化学式中标记硅元素的化合价H2$\stackrel{+4}{Si}$O3.
⑤矿泉水属于混合物(填“纯净物”或“混合物”).
⑥淡水资源有限,我们需要节约用水,如图中表示节水标志的是

20.我州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品9.0g于烧杯中,将50g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下.
请计算:
(1)X的值为1.5.
(2)该石灰石样品中碳酸钙的质量分数为83.3%.
(3)所用稀盐酸溶质的质量分数.(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸质量/g | 10 | 10 | 10 | 10 | 10 |
| 剩余固体质量/g | 7.0 | 5.0 | 3.0 | 1.5 | X |
(1)X的值为1.5.
(2)该石灰石样品中碳酸钙的质量分数为83.3%.
(3)所用稀盐酸溶质的质量分数.(写出计算过程)
4.上述溶液为饱和溶液的是( )
| A. | ②③④ | B. | ②④ | C. | ③④ | D. | ④ |
5.活性炭能净水,主要是因为它具有( )
| A. | 难溶性 | B. | 稳定性 | C. | 吸附性 | D. | 可燃性 |