题目内容
1.某兴趣小组在实验室发现了标本,查阅资料知其主要成分是Cu2(OH)2CO3.他们以Cu2(OH)2CO3为原料制取铜,其工艺流程如图所示.
(1)过滤操作中用到的铁制仪器为铁架台.
(2)无色气体A的化学式是CO2,大气中该气体含量不断上升,会导致温室效应增强,全球气候变暖.
(3)写出蓝色溶液B与铁粉发生反应的化学方程式Fe+CuSO4═FeSO4+Cu.
(4)试剂E可选用稀硫酸溶液.
(5)Cu2(OH)2CO3与稀硫酸发生化学方程式为Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑.
分析 (1)根据过滤操作所需的仪器,进行分析解答.
(2)Cu2(OH)2CO3与稀硫酸反应生成硫酸铜、水和二氧化碳,进行分析解答.
(3)蓝色溶液B为硫酸铜溶液,与过量铁粉反应生成硫酸亚铁溶液和铜,进行分析解答.
(4)固体C为铁粉与铜的混合物,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,进行分析解答.
(5)Cu2(OH)2CO3与稀硫酸反应生成硫酸铜、水和二氧化碳,写出反应的化学方程式即可.
解答 解:(1)过滤操作中用到的铁制仪器为铁架台.
(2)Cu2(OH)2CO3与稀硫酸反应生成硫酸铜、水和二氧化碳,无色气体A的化学式是CO2;大气中该气体含量不断上升,会导致温室效应增强,全球气候变暖.
(3)蓝色溶液B为硫酸铜溶液,与铁粉反应生成硫酸亚铁溶液和铜,反应的化学方程式为Fe+CuSO4═FeSO4+Cu.
(4)固体C为铁粉与铜的混合物,铁能与稀硫酸反应生成硫酸亚铁溶液和氢气,试剂E可选用稀硫酸.
(5)Cu2(OH)2CO3与稀硫酸反应生成硫酸铜、水和二氧化碳,反应的化学方程式为:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑.
故答案为:(1)铁架台;(2)CO2;温室效应;(3)Fe+CuSO4═FeSO4+Cu;(4)稀硫酸;(5)Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑.
点评 本题难度不大,理解以Cu2(OH)2CO3为原料制取铜的工艺流程,掌握金属的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
相关题目
1. 中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上可用如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )
中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上可用如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )
 中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上可用如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )
中国最新战机歼-31使用了高强度、耐高温的钛合金材料.工业上可用如下:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.下列有关该反应的说法正确的是( )| A. | Mg比Ti活泼 | B. | Mg的化合价降低 | ||
| C. | 该反应可以在空气中进行 | D. | 该反应是复分解反应 |
2.下列图示实验操作中,正确的是( )
| A. | 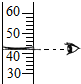 读液体体积 | B. | 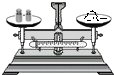 称量固体质量 | C. | 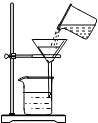 过滤 | D. | 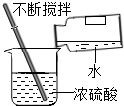 稀释浓硫酸 |
19.化学式是一种用元素符号表示物质组成的式子,下列化学式与它所代表的含义的解释对应不正确的是( )
| A. | H2-氢气 | B. | 4Fe-四个铁原子 | ||
| C. | Cl--氯离子 | D. | 2CO2-两个二氧化碳原子 |
6.如图所示的实验中,得出的结论不正确的是( )
| A. | 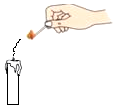 蜡烛刚熄灭时产生的白烟能燃烧,说明白烟具有可燃性 | |
| B. | 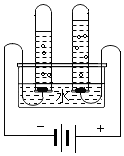 电解水实验能生成氮气和氧气,说明水是由氮元素和氧元素构成的 | |
| C. | 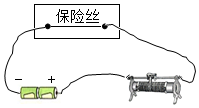 电流过大时,保险丝会自动熔断,说明此时通过保险丝的电流大于保险丝能承受的最大电流 | |
| D. | 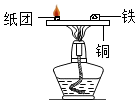 纸团燃烧而铁不燃烧,说明纸的着火点高于铁的着火点 |
13.实验室常用下列装置来制取、收集气体.请阅读资料卡,回答有关问题.

(1)仪器a、b的名称是锥形瓶、集气瓶.
(2)实验室制取和收集甲烷的装置组合是AC或AD;将反应物装入试管前,应先检查装置的气密性.点燃甲烷前一定要先检验甲烷的纯度.
(3)通过对实验室制取气体的学习,你认为实验室制取气体的反应,共同点是cd(填序号).
a.需要加热 b.需要催化剂 c.反应物中没有气体参加 d.反应物中必须含有要制取物质的元素
(4)根据物质的组成对甲烷分类,它属于有机化合物,具有的物理性质是通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水.甲烷除用作燃料外,还是一种很重要的化工原料,在催化剂的作用下,可以将COx和CH4的混合气体直接转化为醋酸(CH3COOH).若该反应的原子利用率为100%(反应物中的原子全部转化为目标产物中的原子),则COx中的x为2,该反应类型是化合反应.
| 资料: 1.第八届国际天然气水合物大会于2014年7月29日在北京召开.据中国地质调查局相关负责人透露,我国计划于2015年开始着手开发“可燃冰”.“可燃冰”主要成分是甲烷水合物,主要分布于深海沉积物或陆域的永久冻土中,1立方米的“可燃冰”可在常温下释放164立方米的甲烷和0.8立方米的淡水,被认为是有一种潜力较大的能源之一. 2.通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水,很容易燃烧.甲烷的实验室制法是:用无水醋酸钠和碱石灰两种固态药品,经研磨均匀混合后装入试管中,加热产生甲烷气体. |

(1)仪器a、b的名称是锥形瓶、集气瓶.
(2)实验室制取和收集甲烷的装置组合是AC或AD;将反应物装入试管前,应先检查装置的气密性.点燃甲烷前一定要先检验甲烷的纯度.
(3)通过对实验室制取气体的学习,你认为实验室制取气体的反应,共同点是cd(填序号).
a.需要加热 b.需要催化剂 c.反应物中没有气体参加 d.反应物中必须含有要制取物质的元素
(4)根据物质的组成对甲烷分类,它属于有机化合物,具有的物理性质是通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水.甲烷除用作燃料外,还是一种很重要的化工原料,在催化剂的作用下,可以将COx和CH4的混合气体直接转化为醋酸(CH3COOH).若该反应的原子利用率为100%(反应物中的原子全部转化为目标产物中的原子),则COx中的x为2,该反应类型是化合反应.
10.如表是部分食品的pH,有关说法错误的是( )
| 食物 | 苹果汁 | 葡萄汁 | 牛奶 | 鸡蛋清 |
| pH | 2.9~3.3 | 3.5~4.5 | 6.3~6.6 | 7.6~8.0 |
| A. | 牛奶和鸡蛋清显碱性 | B. | 苹果汁和葡萄汁显酸性 | ||
| C. | 苹果汁比葡萄汁的酸性强 | D. | 胃酸过多的人应该少喝苹果汁 |
11.甲和乙分别是氢气和一氧化碳还原氧化铜的实验,下列有关说法正确的是( )


| A. | 甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应 | |
| B. | 乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 | |
| C. | 甲、乙两实验中,都应先使试管、玻璃管均匀受热,再通入气体,以防止发生爆炸 | |
| D. | 甲实验试管口向下倾斜可防止反应生成的水倒流 |