题目内容
一种碳酸盐的矿石,其主要成分是BaCO温度 0℃ 50℃ 80℃
Ca(OH)2溶解度 0.173 0.130 0.094
Ba(OH)2溶解度 1.64 13.1 101.5
根据上述信息,为了将矿石中的CaCO![]() 除去,按下列图示进行处理:
除去,按下列图示进行处理:

完成下列填空:
(1)写出实现上述各步变化的方法:
①________②________③________④________
(2)写出步骤④的化学反应方程式:________。
答案:
解析:
提示:
解析:
| 分析:利用信息解决一些具体问题是近年来考查学生能力的一种新题型,是考查自学能力、理解能力和综合解决具体问题能力的最好形式。首先应认真阅读题目所给的信息,同时加以分析理解,正确运用所给的知识解决问题。从本题看给出的信息为
①BaCO BaCO CaCO ②BaO、CaO具有相似的化学性质,都能与水反应生成相应的碱 BaO+H CaO+H ③Ba(OH)、Ca(OH) 根据上述三点信息,即可解决本题。 答案:(1)①高温煅烧
②溶解于水 ③加热过滤 ④通入适量CO (2)Ba(OH)
|
提示:

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
有一种碳酸盐的矿石,其主要成分为BaCO3和CaCO3,这两种盐具有相似的性质:都难溶于水;高温煅烧都可以分解成为氧化物.钡和钙元素的氧化物或氢氧化物也有相似的化学性质,但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度.
小明根据上述信息,设计出除去矿石中CaCO3得到较纯净的BaCO3的实验流程图.

(1)请你在空白的方框中填上相应的物质的化学式.
(2)写出①②④中含钡元素物质发生反应的化学方程式.
① ;
② ;
④ .
(3)请你推测③的操作方法 .
| 温度/℃ | 0 | 40 | 80 |
| Ca(OH)2溶解度/g | 0.187 | 0.141 | 0.094 |
| Ba(OH)2溶解度/g | 1.67 | 8.22 | 101.4 |

(1)请你在空白的方框中填上相应的物质的化学式.
(2)写出①②④中含钡元素物质发生反应的化学方程式.
①
②
④
(3)请你推测③的操作方法
有一种碳酸盐的矿石,其主要成分为BaCO3和CaCO3.某工厂用这种矿石生产得到BaCO3和NaOH.生产流程如图所示.

回答下列问题:
(1)写出第①、②步发生反应的化学方程式:
①
②
(2)80℃下过滤的原因是 .
(3)第④步加入A盐的化学式是 .

| 温度/℃ 溶解度/g 物质 |
0 | 40 | 80 |
| Ca(OH)2 | 0.187 | 0.141 | 0.094 |
| Ba(OH)2 | 1.67 | 8.22 | 101.4 |
(1)写出第①、②步发生反应的化学方程式:
①
②
(2)80℃下过滤的原因是
(3)第④步加入A盐的化学式是
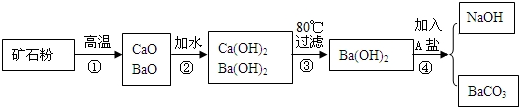
有一种碳酸盐的矿石,其主要成分为BaCO3和CaCO3.某工厂用这种矿石生产得到BaCO3和NaOH.生产流程如图所示.
| 温度/℃ 溶解度/g 物质 | 0 | 40 | 80 |
| Ca(OH)2 | 0.187 | 0.141 | 0.094 |
| Ba(OH)2 | 1.67 | 8.22 | 101.4 |
(1)写出第①、②步发生反应的化学方程式:
①______
②______
(2)80℃下过滤的原因是______.
(3)第④步加入A盐的化学式是______.


