题目内容
11.如图1是甲、乙两种物质的溶解度曲线,如图2所示两个烧杯中各盛有20℃时两种物质的饱和溶液.请你通过分析,回答下列问题:
(1)下列方法中能使甲物质的溶解度增大的是B.
A.溶解时搅拌 B.升高温度 C.降低温度 D.增加水的质量
(2)在80℃时,将55克甲物质放到50克水中,形成溶液的质量是100克.
(3)不改变溶质质量分数使接近饱和的乙的不饱和溶液变为饱和溶液的方法是升温.
(4)当温度由20℃升高到60℃时(不考虑水分蒸发),B烧杯中固体质量增多,则B烧杯溶液中的溶质是乙(填“甲”或“乙”).
(5)将80℃的甲、乙饱和溶液降温到40℃,得到的溶液中溶质的质量分数大小关系是甲>乙(填“>”、“=”或“<”).
(6)甲中含有少量乙时,提纯甲的方法是降温结晶.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)甲物质的溶解度随温度的升高而增大,所以能使甲物质的溶解度增大的是升高温度,故选:B;
(2)在80℃时,A物质的溶解度是100g,所以将55克甲物质放到50克水中,形成溶液的质量是100g;
(3)乙物质的溶解度随温度的升高减小,所以不改变溶质质量分数使接近饱和的乙的不饱和溶液变为饱和溶液的方法是升温;
(4)乙物质的溶解度随温度的升高减小,当温度由20℃升高到60℃时(不考虑水分蒸发),B烧杯中固体质量增多,则B烧杯溶液中的溶质是乙;
(5)80℃时甲物质的溶解度大于40℃时,乙物质的溶解度,所以将80℃的甲、乙饱和溶液降温到40℃,得到的溶液中溶质的质量分数大小关系是甲>乙;
(6)甲物质的溶解度随温度的升高而增大,所以甲中含有少量乙时,提纯甲的方法是降温结晶.
故答案为:(1)B;
(2)100;
(3)升温;
(4)乙;
(5)>;
(6)降温结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
9.材料是时代进步的重要标志.下列有关材料的说法中,错误的是( )
| A. | 棉花属于合成纤维 | |
| B. | 塑料属于有机合成高分子材料 | |
| C. | 不锈钢属于金属材料 | |
| D. | 开发使用可降解塑料,能有效解决“白色污染”问题 |
10.下列物质的名称、俗名与化学式完全对应的是( )
| A. | 氢氧化钙 熟石灰 CaO | B. | 汞 水银 Hg | ||
| C. | 碳酸氢钠 苏打 NaHCO3 | D. | 碳酸钠 烧碱 Na2CO3 |
6. 如图装置所示,经数小时后,U形管A、B两处的液面将会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封)( )
如图装置所示,经数小时后,U形管A、B两处的液面将会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封)( )
 如图装置所示,经数小时后,U形管A、B两处的液面将会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封)( )
如图装置所示,经数小时后,U形管A、B两处的液面将会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封)( )| A. | A处上升,B处下降 | B. | A、B两处都下降 | C. | A处下降,B处上升 | D. | A、B两处都不变 |
3.下列关于资源能源叙述错误的是( )
| A. | 煤、石油和天然气是化石燃料且不可再生,我们要节约能源 | |
| B. | 空气是一种宝贵的资源,它主要是由氧气和氮气组成的 | |
| C. | 氢能 源没有污染、燃烧放热多,来源广并且成本低,现已普及使用 | |
| D. | 使用乙醇汽油既节约石油资源、又能减少污染空气还能促进农业生产 |
20.规范实验操作是获得实验成功的重要保证,如图实验操作中正确的是( )
| A. |  倾倒液体 | B. |  检查气密性 | C. |  过滤 | D. |  闻气味 |
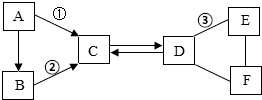 A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)
A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去) 刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.