题目内容
12.实验课上,某小组的同学用生石灰进行“化学反应中能量的变化”实验时发现:向块状生石灰中加入适量水后没有明显的温度变化.为确定其原因,进行了如下实验探究.【提出问题】生石灰是否变质?其成分是什么?
【查阅资料】氢氧化钙溶解过程中无明显温度变化,与盐酸反应无气体生成.
【猜想与假设】同学们认为生石灰样品已经变质,并对其成分作出了如下4种猜想.
猜想1:氧化钙和氢氧化钙;
猜想2:氧化钙和碳酸钙;
猜想3:Ca(OH)2 和CaCO3;
猜想4:氧化钙、氢氧化钙和碳酸钙.
【进行实验】同学们将少量样品研碎后,按如图所示过程进行实验.
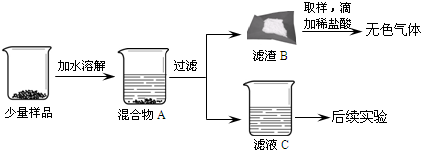
(1)在溶解过程中用温度计测量液体的温度,发现温度计示数升高,说明样品中应该含有CaO.
结论:猜想3不成立.
(2)滤渣B中一定含有CaCO3,用化学方程式表示生成该物质的反应CO2+Ca(OH)2═CaCO3↓+H2O.
结论:①块状生石灰表面发生变质;②猜想1不成立.
(3)为验证滤液C的成分,进行后续实验.
分析 【猜想与假设】猜想3:根据题中的其他猜想来完成解答;
【进行实验】(1)根据题中的查阅资料可以完成解答;
(2)向滤渣B中加入稀盐酸产生了气体,所以可以判断在滤渣中含有碳酸钙,可以据此解答该题.
解答 解:【猜想与假设】猜想3:根据题中的其他猜想结合氧化钙的性质可以知道,该固体可能是氢氧化钙和碳酸钙;
【进行实验】(1)根据题中的查阅资料可以知道,氢氧化钙溶于水时温度变化不大,而本实验中液体明显升温,所以可以判断该物质中含有氧化钙;
(2)向滤渣B中加入稀盐酸产生了气体,所以可以判断在滤渣中含有碳酸钙,氢氧化钙可以和二氧化碳反应生成碳酸钙,该反应的化学方程式为:CaCO3CO2+Ca(OH)2═CaCO3↓+H2O;
故答案为:【猜想与假设】猜想3:Ca(OH)2 和CaCO3;
【进行实验】(1)CaO;
(2)CaCO3;CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本题综合考查生石灰氧化钙、熟石灰氢氧化钙的性质及碳酸根离子的检验,通过实验探究解决问题,综合性较强,要求学生具有分析和解决问题的能力.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
2. 向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图所示曲线表示的是( )
向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图所示曲线表示的是( )
 向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图所示曲线表示的是( )
向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图所示曲线表示的是( )| 序号 | 甲 | 乙 |
| ① | 铜、锌的混合物 | 稀盐酸 |
| ② | 硫酸和硫酸铜的混合溶液 | 氢氧化钠溶液 |
| ③ | 盐酸和稀硫酸的混合溶液 | 氯化钡溶液 |
| ④ | 生锈的铁钉 | 稀盐酸 |
| A. | ②③ | B. | ①② | C. | ②④ | D. | ③④ |
7.下表是小江同学用多种方法来鉴别物质的情况,其中完全正确的是C
A.A B.B C.C D.锌.
| 需鉴别物质 | 所加试剂或方法 | ||
| 方法1 | 方法2 | ||
| A | 木炭粉和氧化铜 | 观察颜色 | 通CO并加热 |
| B | NaCl溶液和Na2CO3溶液 | 稀HCl | Zn |
| C | NH4HCO3和K2SO4 | 加Ca(OH) 2研磨并闻气味 | 稀H 2SO 4 |
| D | 稀HCl和NaCl溶液 | 加紫色石蕊试液 | |
17.某工厂按如下步骤进行生产:
(1)以煤为燃料煅烧石灰石;
(2)用饱和Na2CO3溶液充分吸收步骤(1)中产生的CO2,发生的反应为:Na2CO3+CO2+H2O═2NaHCO3;
(3)使步骤(1)中产生的CaO与水反应;
(4)用得到的产物与Na2CO3溶液反应,
该厂生产过程中没有涉及的化学反应类型是( )
(1)以煤为燃料煅烧石灰石;
(2)用饱和Na2CO3溶液充分吸收步骤(1)中产生的CO2,发生的反应为:Na2CO3+CO2+H2O═2NaHCO3;
(3)使步骤(1)中产生的CaO与水反应;
(4)用得到的产物与Na2CO3溶液反应,
该厂生产过程中没有涉及的化学反应类型是( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
4.下列过程中主要涉及物理变化的是( )
| A. | 浓硫酸使白纸变黑 | B. | 用浓硫酸来干燥潮湿的氧气 | ||
| C. | 用熟石灰处理硫酸厂的污水 | D. | 盐酸使紫色石蕊溶液变红色 |
2.世界万物都是由各种元素组成的,请从O、S、H、Na这四种元素中选择适当的元素组成物质,写出符合下列要求的化学式(每空只要求写一个).
| 物质类别 | 酸 | 碱 | 盐 |
| 化学式 | H2SO4 | NaOH | Na2SO4 |
 (1)试用两种不同的方法区分一氧化碳和二氧化碳两种无色气体,简述实验方法和实验现象.
(1)试用两种不同的方法区分一氧化碳和二氧化碳两种无色气体,简述实验方法和实验现象.