题目内容
以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:
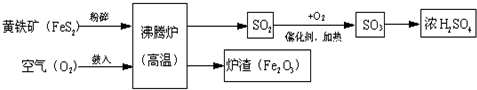
(1)写出流程图中一种氧化物的名称 .
(2)将黄铁矿粉碎,目的是 .
(3)流程中SO2转化为SO3的化学方程式为 .
(4)实验室稀释浓硫酸应注意什么? .
(5)炉渣(Fe2O3)在工业上可用来 写出工业上以Fe2O3 为原料生产铁的化学方程式 .

(1)写出流程图中一种氧化物的名称
(2)将黄铁矿粉碎,目的是
(3)流程中SO2转化为SO3的化学方程式为
(4)实验室稀释浓硫酸应注意什么?
(5)炉渣(Fe2O3)在工业上可用来
考点:物质的相互转化和制备,浓硫酸的性质及浓硫酸的稀释,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)氧化物是由两种元素组成,一种元素是氧元素的化合物;
(2)黄铁矿粉碎会增大反应物的接触面积加快反应速度;
(3)根据化学方程式的书写考虑;
(4)根据浓硫酸的稀释方法考虑;
(5)根据氧化铁可以用来炼铁考虑.
(2)黄铁矿粉碎会增大反应物的接触面积加快反应速度;
(3)根据化学方程式的书写考虑;
(4)根据浓硫酸的稀释方法考虑;
(5)根据氧化铁可以用来炼铁考虑.
解答:解:(1)二氧化硫或三氧化硫或三氧化二铁都是由两种元素组成,一种元素是氧元素,属于氧化物;
(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度;
(3)反应物是二氧化硫和氧气,生成物是三氧化硫,用观察法配平,反应条件是催化剂和加热,所以方程式是:2SO2+O2
2SO3;
(4)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌;
(5)炉渣(Fe2O3)可以用来炼铁,一氧化碳与氧化铁反应生成铁和二氧化碳,所以可以用做冶铁原料,反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,根据得失氧进行配平,反应条件是高温,所以方程式是:3CO+Fe2O3
2Fe+3CO2.
故答案为:(1)二氧化硫(或三氧化硫或三氧化二铁);(2)增大反应物的接触面积;(3)2SO2+O2
2SO3;(4)将浓硫酸沿器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中;(5)炼铁;3CO+Fe2O3
2Fe+3CO2.
(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度;
(3)反应物是二氧化硫和氧气,生成物是三氧化硫,用观察法配平,反应条件是催化剂和加热,所以方程式是:2SO2+O2
| ||
| △ |
(4)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌;
(5)炉渣(Fe2O3)可以用来炼铁,一氧化碳与氧化铁反应生成铁和二氧化碳,所以可以用做冶铁原料,反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,根据得失氧进行配平,反应条件是高温,所以方程式是:3CO+Fe2O3
| ||
故答案为:(1)二氧化硫(或三氧化硫或三氧化二铁);(2)增大反应物的接触面积;(3)2SO2+O2
| ||
| △ |
| ||
点评:解答本题的关键是要知道氧化物的特点,知道反应物接触面积越大,反应越剧烈,熟悉方程式的书写注意事项,知道浓硫酸的稀释方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在四只小烧杯中分别放入浓度相同的稀盐酸各20克,然后向其中分别加入足量的下列物质,经充分反应,所得溶液溶质的质量分数最大的是( )
| A、Mg |
| B、MgO |
| C、Mg(OH)2 |
| D、MgCO3 |
下图所示的实验中,发生了化学变化的是( )
A、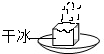 干冰升华 |
B、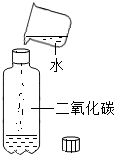 CO2溶于水 |
C、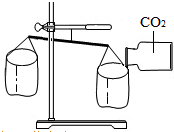 实验CO2的密度 |
D、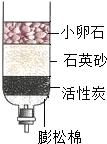 自制过滤器过滤液体 |