题目内容
实验室用足量的一氧化碳还原氧化铜,若要得到4g的铜,参加反应的一氧化碳质量为多少克?
分析:欲正确解答本题,需根据化学方程式得出各物质之间的质量比,列出比例式,通过计算得出所需物质的质量.
解答:解:设参加反应的一氧化碳质量为x
CuO+CO
Cu+CO2
28 64
x 4g
=
X=1.75g
答:参加反应的一氧化碳质量为1.75克;
CuO+CO
| ||
28 64
x 4g
| 28 |
| x |
| 64 |
| 4g |
X=1.75g
答:参加反应的一氧化碳质量为1.75克;
点评:本题考查学生根据化学反应方程式进行计算的解题能力,必须掌握正确的计算步骤和格式.

练习册系列答案
相关题目
小强同学在化学实验室发现一瓶盛有白色粉末的试剂瓶,其标签严重破损.老师告诉他,这瓶试剂可能是硫酸钠、碳酸钠、碳酸氢钠中的一种.小强同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
| 物质 | Na2SO4 | Na2CO3 | NaHCO3 |
| 溶解度/g | 19.5 | 21.5 | 9.6 |
(2)为确定其成分,小强该同学对此溶液继续进行如下实验探究:
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量溶液于试管中,加稀盐酸 | 溶液有气泡产生 | 该溶液是________溶液 |
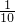 与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?( 用到的化学方程式:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH )
小强同学在化学实验室发现一瓶盛有白色粉末的试剂瓶,其标签严重破损.老师告诉他,这瓶试剂可能是硫酸钠、碳酸钠、碳酸氢钠中的一种.小强同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
(1)小强同学在常温下把10.6g的白色粉末加入100g水中,发现粉末全部溶解.根据上述信息.分析认为此溶液一定不是______溶液.该溶液的溶质质量分数为______.
(2)为确定其成分,小强该同学对此溶液继续进行如下实验探究:
(3)小强同学取(1)配制的溶液的 与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
( 用到的化学方程式:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH )
| 物质 | Na2SO4 | Na2CO3 | NaHCO3 |
| 溶解度/g | 19.5 | 21.5 | 9.6 |
(2)为确定其成分,小强该同学对此溶液继续进行如下实验探究:
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量溶液于试管中,加稀盐酸 | 溶液有气泡产生 | 该溶液是______溶液 |
 与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?( 用到的化学方程式:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH )
小强同学在化学实验室发现一瓶盛有白色粉末的试剂瓶,其标签严重破损.老师告诉他,这瓶试剂可能是硫酸钠、碳酸钠、碳酸氢钠中的一种.小强同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
(1)小强同学在常温下把10.6g的白色粉末加入100g水中,发现粉末全部溶解.根据上述信息.分析认为此溶液一定不是______溶液.该溶液的溶质质量分数为______.
(2)为确定其成分,小强该同学对此溶液继续进行如下实验探究:
(3)小强同学取(1)配制的溶液的 与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
( 用到的化学方程式:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH )
| 物质 | Na2SO4 | Na2CO3 | NaHCO3 |
| 溶解度/g | 19.5 | 21.5 | 9.6 |
(2)为确定其成分,小强该同学对此溶液继续进行如下实验探究:
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量溶液于试管中,加稀盐酸 | 溶液有气泡产生 | 该溶液是______溶液 |
 与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?
与足量的氢氧化钡溶液反应,理论上能产生多少克沉淀?( 用到的化学方程式:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH )

