题目内容
14.小华家里有一小袋粗盐,有一天他发现敞口放置的粗盐表面有溶解现象.经查阅资料得知,这种现象在化学上叫潮解,原因是粗盐中含有氯化钙和氯化镁.于是他设计了以下实验方案对精盐进行提纯.请回答有关问题.(1)将粗盐全部溶于水,加入过量的氢氧化钠溶液,其主要目的是除去粗盐中的除去氯化镁.
(2)再加入过量碳酸钠溶液,目的是除去粗盐中的氯化钙.
(3)待充分反应后过滤,向滤液中加入适量的稀盐酸,目的是除去反应中过量的氢氧化钠和碳酸钠,完全反应后,加热、蒸发、结晶,得到几乎不含其它杂质的氯化钠晶体;
(4)写出以上各步骤中其中一个反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 (1)根据氢氧化钠会与氯化镁反应生成沉淀进行分析;
(2)根据碳酸钠会与氯化钙反应生成转化为沉淀进行分析;
(3)根据加入的氢氧化钠、碳酸钠都是过量的,会对氯化钠造成影响进行分析;
(4)根据题中各物质之间的反应进行分析.
解答 解:(1)氢氧化钠会与氯化镁反应生成氢氧化镁沉淀和氯化钠,所以加入过量的氢氧化钠溶液,其主要目的是:除去氯化镁;
(2)碳酸钠会与氯化钙反应生成碳酸钙沉淀和氯化钠,所以加入过量的碳酸钠溶液,目的是除去粗盐中的氯化钙;
(3)加入的氢氧化钠、碳酸钠都是过量的,会对氯化钠造成影响,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,氢氧化钠和盐酸反应生成氯化钠和水,所以向滤液中加入适量盐酸,目的是:除去反应中过量的氢氧化钠和碳酸钠;
(4)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)除去氯化镁;
(2)氯化钙;
(3)除去反应中过量的氢氧化钠和碳酸钠;
(4)Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题主要对物质的除杂和净化进行了探究,在除杂质的同时不要引入新的杂质.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
4.恰当的安全措施能减少生命财产损失.下列事故处理措施正确的是( )
| A. | 高层住房内着火,立即打开所有门窗 | |
| B. | 电器着火,立即用水扑灭 | |
| C. | 油锅着火,立即盖上锅盖 | |
| D. | 煤气泄露,立即打开排气扇的电源开关 |
5.下列物质敞口放置在空气中,溶质发生变质且溶液质量增加的是( )
| A. | 石灰水 | B. | 氢氧化钠溶液 | C. | 浓盐酸 | D. | 浓硫酸 |
2.下列物质的用途,不正确的是( )
| A. | 盐酸用于除铁锈 | B. | 干冰用于人工降雨 | ||
| C. | 金刚石用于刻划玻璃 | D. | 熟石灰用于治疗胃酸过多 |
9.如表是某指示剂在一定pH范围内所显示的颜色:
向滴有少量该指示剂的NaOH溶液中加入稀盐酸,有可能出现的颜色变化是( )
| 颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
| pH | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
| A. | 由紫到绿 | B. | 由绿到蓝 | C. | 由橙到绿 | D. | 由红到紫 |
19.下列实验操作中,不能达到实验目的是( )
| 物质 | 实验目的 | 主要实验操作 | |
| A | H2O和H2O2 | 鉴别 | 加入适量二氧化锰,观察是否有气泡产生 |
| B | MnO2(KCl) | 分离 | 溶解、过滤、蒸发 |
| C | CO2(H2O) | 干燥 | 将气体通过碱石灰(主要成分氢氧化钠)干燥管 |
| D | NaOH、Ca(OH)2 | 除杂 | 加入适量Na2CO3溶液,充分反应后,过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
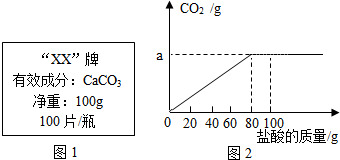 钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
 ,则X=8.
,则X=8. 为测定由盐酸和硫酸组成的某混合酸中溶质的质量分数,取100g该混合酸,逐滴加入某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图所示.
为测定由盐酸和硫酸组成的某混合酸中溶质的质量分数,取100g该混合酸,逐滴加入某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图所示.