题目内容
某固体可能由Na2SO4,NaCl,Na2CO3,KNO3中的一种或几种组成,现进行如下实验:

试回答:
(1)白色沉淀A的化学式为 ;
(2)原固体中一定含有 ,一定不含有 ,可能含有 ;
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:(请补充完整)取少量固体溶于水, .

试回答:
(1)白色沉淀A的化学式为
(2)原固体中一定含有
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:(请补充完整)取少量固体溶于水,
考点:物质的鉴别、推断,盐的化学性质
专题:混合物组成的推断题
分析:根据白色沉淀可以溶于硝酸生成气体的性质即可判定它是碳酸钡,以此为突破口,逐一分析,即可正确解答.
解答:解:(1)①Na2SO4和Na2CO3都可与BaCl2发生反应,分别生成硫酸钡和碳酸钡沉淀,但硫酸钡不溶于硝酸,故可判断白色沉淀A为碳酸钡,其化学式为BaCO3;
(2)由(1)①的分析可知,原固体中一定含有碳酸钠,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,由图示可知“B中的酸根离子只有一种”,故原固体中可能含有氯化钠,则一定不含有 Na2SO4,KNO3.
(3)②中加入足量的Ba(NO3)2溶液,碳酸钠与硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠;充分反应后过滤,取滤液加入硝酸银溶液,若含有氯化钠产生白色沉淀.
故答案:(1)BaCO3;
(2)Na2CO3;Na2SO4、KNO3;NaCl;
(3)加入足量的Ba(NO3)2溶液,充分反应后过滤,取滤液加入硝酸银溶液,观察是否有沉淀.
(2)由(1)①的分析可知,原固体中一定含有碳酸钠,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,由图示可知“B中的酸根离子只有一种”,故原固体中可能含有氯化钠,则一定不含有 Na2SO4,KNO3.
(3)②中加入足量的Ba(NO3)2溶液,碳酸钠与硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠;充分反应后过滤,取滤液加入硝酸银溶液,若含有氯化钠产生白色沉淀.
故答案:(1)BaCO3;
(2)Na2CO3;Na2SO4、KNO3;NaCl;
(3)加入足量的Ba(NO3)2溶液,充分反应后过滤,取滤液加入硝酸银溶液,观察是否有沉淀.
点评:此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案
相关题目
以下是小伟同学实验报告中摘录的部分数据,你认为实验数据记录正确的是( )
| A、用量筒量取食盐溶液5.86mL |
| B、用20mL酒精和20mL蒸馏水配制成40mL酒精溶液 |
| C、用广泛pH试纸测得某硫酸溶液的pH=1.4 |
| D、用托盘天平称取明矾22.4g |
 如图所示,A~H是初中化学常见的物质,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂,Y为单质.
如图所示,A~H是初中化学常见的物质,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂,Y为单质. 如图化学反应的溶液颜色变化体现红色溶液了“魔法世界,魅力化学”,请回答:
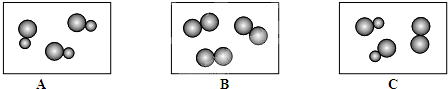
如图化学反应的溶液颜色变化体现红色溶液了“魔法世界,魅力化学”,请回答: ”、“
”、“ ”表示不同元素的原子,请用序号填空:
”表示不同元素的原子,请用序号填空: