题目内容
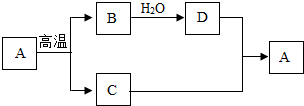
 A、B、C、D、E、F是初中化学内容所涉及到的物质,其中A、B是氧化物,在一定条件下,它们的转化关系如图所示,推断:
A、B、C、D、E、F是初中化学内容所涉及到的物质,其中A、B是氧化物,在一定条件下,它们的转化关系如图所示,推断:(1)C的化学式为
(2)D物质在在空气中缓慢氧化,生成物质主要是B,则B的化学式为
(3)写出D与稀硫酸反应的化学方程式
考点:物质的鉴别、推断,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据亚铁离子溶液属于浅绿色,D与硫酸反应生成浅绿色溶液F和气体E,所以D是金属铁,E是氢气;D物质在在空气中缓慢氧化,生成物质主要是B,则为铁生锈的过程,可知B是三氧化二铁,再根据A属于氧化物,且具有还原性,推出A物质是一氧化碳,根据方程式的写法写出化学方程式.
解答:解:因为亚铁离子溶液属于浅绿色,D与硫酸反应生成浅绿色溶液F和气体E,所以F是亚铁离子溶液,金属与硫酸反应能生成盐和氢气,所以D属于铁就符合条件,铁与硫酸反应生成硫酸亚铁和氢气,D物质在在空气中缓慢氧化,生成物质主要是B,则为铁生锈的过程,可知B是三氧化二铁,而A、B反应生成铁,说明A具有还原性,三大还原剂有:氢气、一氧化碳、碳,A属于氧化物,所以A是一氧化碳,一氧化碳与三氧化二铁反应生成铁和二氧化碳,所以C是二氧化碳;因此:
(1)物质C是二氧化碳,故填:CO2;
(2)D物质在在空气中缓慢氧化,生成物质主要是B,则为铁生锈的过程,可知B是三氧化二铁,则B的化学式为Fe2O3;A和B反应的化学方程式为 3CO+Fe2O3
2Fe+3CO2.
(3)D与稀硫酸反应的反应物是铁和硫酸,生成物是硫酸亚铁和氢气,故化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故答案为:
(1)CO2.
(2)Fe2O3,3CO+Fe2O3
2Fe+3CO2.
(3)Fe+H2SO4═FeSO4+H2↑.
(1)物质C是二氧化碳,故填:CO2;
(2)D物质在在空气中缓慢氧化,生成物质主要是B,则为铁生锈的过程,可知B是三氧化二铁,则B的化学式为Fe2O3;A和B反应的化学方程式为 3CO+Fe2O3
| ||
(3)D与稀硫酸反应的反应物是铁和硫酸,生成物是硫酸亚铁和氢气,故化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故答案为:
(1)CO2.
(2)Fe2O3,3CO+Fe2O3
| ||
(3)Fe+H2SO4═FeSO4+H2↑.
点评:本题为框图式推断题,解答本题关键是找出突破口:D与硫酸反应生成浅绿色溶液F和气体E,推出D是铁,再根据铁燃烧的产物求出B的化学式,根据三大还原剂分析出A物质.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
将含有H2,N2,CO2,CO的混合气体依次通过足量的NaOH溶液,灼热CuO的和浓H2SO4最后剩余的气体是( )
| A、N2 |
| B、N2和CO2 |
| C、H2和CO2 |
| D、H2和N2 |
如图为元素周期表第三周期的一部分,下列说法中正确的是( )

| A、Si元素的名称是硅,其核电荷数为14 |
B、Mg原子的核外电子排布是 |
| C、Al的相对原子质量是26.98g |
| D、它们都属于金属元素 |
如图为钠元素的原子结构示意图,下列说法不正确的是( )


| A、钠原子核外有三个电子层 |
| B、钠原子核外电子总数为11 |
| C、钠原子最外层电子数为1 |
| D、钠原子在化学反应中易得到电子 |
实验室用氯酸钾和高锰酸钾制取氧气,两者的共同点是( )
| A、都生成两种物质 |
| B、都使用二氧化锰做催化剂 |
| C、都是化合反应 |
| D、都是分解反应 |