题目内容
8. 节约用水、保护水资源是每个公民应尽的义务.
节约用水、保护水资源是每个公民应尽的义务.(1)海水、河水、湖水都是天然水,属于混合物(填“纯净物”或“混合物”)
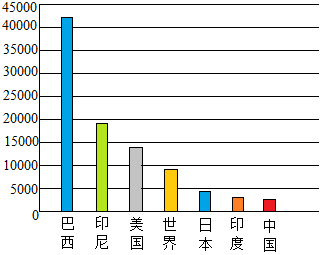
(2)如图是某些国家的人均水量和世界人均水量(m3/人)
由图中可以看出我国是一个水资源短缺(选填
“短缺”或“丰富”)的国家.谈谈你在生活中节约用
水的做法:使用节水龙头(写一条即可)
(3)过滤可以除去水中不溶性的固体杂质,过滤时所需
要的玻璃仪器有烧杯、玻璃棒、漏斗.
(4)在布满小卵石的小河中,河水常常是清澈透明的,其原因是小卵石可以起过滤作用,除去难溶性杂质.
分析 (1)混合物是由不同物质组成的,纯净物是由同种物质的组成的;
(2)根据题意和图示进行分析解答;
(3)根据过滤时用到的玻璃仪器有:烧杯、玻璃棒、漏斗解答;
(4)根据小卵石可以起过滤作用解答.
解答 解:(1)海水、河水、湖水都是天然水,天然水是混合物;
(2)对照图表数据可知,我国是一个水资源短缺的国家.家中的节水办法是:使用节水龙头,洗脸,洗衣水冲厕所等.
(3)过滤时用到的玻璃仪器有:烧杯、玻璃棒、漏斗.
(4)在布满小卵石的小河中,河水常常是清澈透明的,其原因是:小卵石可以起过滤作用,除去难溶性杂质.
故答案为:(1)混合物;
(2)短缺;使用节水龙头;
(3)烧杯、玻璃棒、漏斗;
(4)小卵石可以起过滤作用,除去难溶性杂质.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
19.铅蓄电池在生产、生活中使用广泛.其构造示意图如图1,回答下列问题:
(1)铅蓄电池充电时是将电能转化为c(填序号)
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断增大(填“增大”、“减小”或“不变”).
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类有机合成材料;
②废硫酸可以与氟磷灰石[Ca5(PO4)3F]反应,反应的化学方程式为2Ca5(PO4)3F+7H2SO4═3CaSO4+3Ca(H2PO4)2+2HF,反应产物中可用作化肥的物质是Ca(H2PO4)2.
③废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
已知:2NH3+H2SO4═(NH4)SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择b(填序号).
a、CaCO3 b、Ca(OH)2 c、NH3 d、NaOH.

(1)铅蓄电池充电时是将电能转化为c(填序号)
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断增大(填“增大”、“减小”或“不变”).
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类有机合成材料;
②废硫酸可以与氟磷灰石[Ca5(PO4)3F]反应,反应的化学方程式为2Ca5(PO4)3F+7H2SO4═3CaSO4+3Ca(H2PO4)2+2HF,反应产物中可用作化肥的物质是Ca(H2PO4)2.
③废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
| 物质 | CaCO3 | Ca(OH)2 | NH3 | NaOH |
| 市场参考价(元/kg ) | 1.8 | 2.0 | 6.5 | 11.5 |
a、CaCO3 b、Ca(OH)2 c、NH3 d、NaOH.
20.以下实验方法,可行的是( )
| A. | 向某种溶液中加入硝酸银溶液,产生白色沉淀,证明该溶液中一定有氯离子 | |
| B. | 用玻璃棒蘸取硫酸滴在润湿pH试纸上,测定其pH | |
| C. | 按溶解、过滤、蒸发的操作顺序可以分离BaCl2、BaCO3的混合物 | |
| D. | 用高温加热的方法除去氧化铜中混有的碳粉 |
14.20℃时,100g A物质的溶液,温度不变,蒸发掉10g水后有2g A析出,又蒸发掉10g水有4g A析出,则:20℃时A物质的溶解度为( )
| A. | 20g | B. | 40 g | C. | 30 g | D. | 无法计算 |
15.下列关于氧气的说法中正确的是( )
| A. | 氧气能支持燃烧,可作燃料 | |
| B. | 氧气可用于动植物呼吸、医疗急救等 | |
| C. | 氧气的化学性质很活泼,在常温下能与所有物质发生化学反应 | |
| D. | 氧气从淡蓝色液体变成无色气体发生了化学变化 |
 科学家近年在-100℃的低温下合成了一种化合物X,此分子的模拟如图所示,其中每个
科学家近年在-100℃的低温下合成了一种化合物X,此分子的模拟如图所示,其中每个 代表一个碳原子,每个
代表一个碳原子,每个 代表一个氢原子,下列说法中正确的是B
代表一个氢原子,下列说法中正确的是B