题目内容
16.过氧化氢分解的产物与其他物质有如下转换关系.请根据所学知识按要求填空: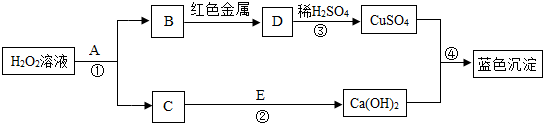
(1)物质A在反应①中起催化作用.
(2)②的化学反应方程式为CaO+H2O=Ca(OH)2属于放热(填“吸热”或“放热”)反应.
(3)反应③的化学方程式为CuO+H2SO4=CuSO4+H2O.
分析 根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以A是二氧化锰,C会与E反应生成氢氧化钙,所以C是水,B是氧气,氧气和红色金属铜在加热的条件下生成氧化铜,所以D是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,氧化钙和水反应生成氢氧化钙,所以E是氧化钙,氢氧化钙和硫酸铜反应生成氢氧化铜沉淀和硫酸钙,然后将推出的物质进行验证即可.
解答 解:(1)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以A是二氧化锰,C会与E反应生成氢氧化钙,所以C是水,B是氧气,氧气和红色金属铜在加热的条件下生成氧化铜,所以D是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,氧化钙和水反应生成氢氧化钙,所以E是氧化钙,氢氧化钙和硫酸铜反应生成氢氧化铜沉淀和硫酸钙,经过验证,推导正确,所以A是二氧化锰,二氧化锰是过氧化氢分解的催化剂,起催化作用;
(2)②是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2,属于放热反应;
(3)反应③是氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4=CuSO4+H2O.
故答案为:(1)催化;
(2)CaO+H2O=Ca(OH)2,放热;
(3)CuO+H2SO4=CuSO4+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
7.探究镁和锌与盐酸反应的快慢,不需要控制的变量是( )
| A. | 两种金属的形状 | B. | 盐酸的质量分数 | C. | 温度 | D. | 反应容器的大小 |
7.酸、碱、盐溶解性表是学习自然科学的重要工具,下表列出了“部分酸、碱、盐在20℃时的溶解性”.请利用此表完成下列任务:
(1)查Mg(OH)2的溶解性:不溶(填“溶”或“不溶”).
(2)用化学方程式表示CuSO4与表中的一种碱的溶液反应2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
| OH- | Cl- | CO32- | SO42- | |
| H+ | 溶、挥 | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Mg2+ | 不溶 | 溶 | 不溶 | 溶 |
| Cu2+ | 不溶 | 溶 | 不溶 | 溶 |
(2)用化学方程式表示CuSO4与表中的一种碱的溶液反应2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
4.以下是根据一些反应事实推理出的影响化学反应的因素,其中推理不合理的是( )
| A. | 双氧水在常温下很难分解,而在加入二氧化锰后迅速分解--催化剂 | |
| B. | 硫在空气中燃烧发出淡蓝色火焰,在纯氧中燃烧发出蓝紫色火焰--反应物浓度 | |
| C. | 食物在冰箱中保存不易腐烂--温度 | |
| D. | 铜片在空气中很难燃烧,铜粉在空气中能燃烧--反应物的种类 |
1. 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )
 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )| A. | t2℃时甲、乙两物质的溶解度相等 | |
| B. | 温度大于t2℃时,甲、乙、丙三种固体物质溶解度的大小关系是甲>乙>丙 | |
| C. | 当甲中混入少量乙时,可用冷却热饱和溶液的方法得到较纯净的甲 | |
| D. | 小于t1℃时甲大于丙 |
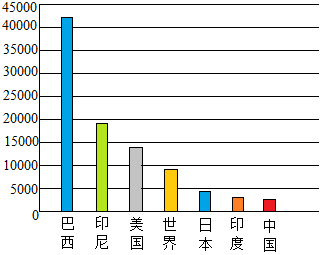 节约用水、保护水资源是每个公民应尽的义务.
节约用水、保护水资源是每个公民应尽的义务.