题目内容
15.化学与生活生产息息相关,请运用化学知识回答以下问题.(1)目前市场上有:高钙奶粉、补锌口服液等,人体缺铁可能会引起贫血.
(2)铝制品抗腐蚀性能很好,原理是4Al+3O2═2Al2O3(用化学方程式表示).
(3)处理硫酸工厂废水Ca(OH)2+H2SO4=CaSO4+2H2O(用化学方程式表示).
(4)军事上烟雾弹的反应原理4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5(用化学方程式表示).
(5)化肥碳铵施用时不可暴晒,暴晒会降低肥效其原因是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑(用化学方程式表示).
分析 (1)根据铁的生理功能和缺乏症进行分析解答.
(2)铝具有良好的抗腐蚀性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,写出反应的化学方程式即可.
(3)可用熟石灰处理硫酸工厂废水,熟石灰和硫酸反应生成硫酸钙和水,写出反应的化学方程式即可.
(4)红磷在空气中燃烧生成五氧化二磷,该反应产生大量的白烟,写出反应的化学方程式即可.
(5)碳铵化肥在烈日暴晒下分解生成氨气、水和二氧化碳,写出反应的化学方程式即可.
解答 解:(1)铁是合成血红蛋白的主要元素,缺乏会患贫血.
(2)铝具有良好的抗腐蚀性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,反应的化学方程式为:4Al+3O2═2Al2O3.
(3)可用熟石灰处理硫酸工厂废水,熟石灰和硫酸反应生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4=CaSO4+2H2O.
(4)红磷在空气中燃烧生成五氧化二磷,该反应产生大量的白烟,可以做烟雾弹,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(5)碳铵化肥在烈日暴晒下分解生成氨气、水和二氧化碳,反应的化学方程式为:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
故答案为:(1)贫血;(2)4Al+3O2═2Al2O3;(3)Ca(OH)2+H2SO4=CaSO4+2H2O;(4)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;(5)NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑.
点评 本题难度不大,掌握化学元素与人体健康的关系、化学方程式的书写方法是正确解答本题的关键.

| A. | X中只含C、H两种元素 | B. | X中C、H元素质量比为3:1 | ||
| C. | X与CO的相对分子质量之差为16 | D. | 反应前后原子的数目不变 |
| A. | ①④ | B. | ①②③ | C. | ③④ | D. | ①③ |
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】电石与水反应的可燃性气体可能是:氧气、氢气或乙炔(C2H2),同学们做出以上猜想的理论依据是化学反应前后元素的种类不变,大家讨论后一致认为该气体不可能是氧气,原因是氧气不具有可燃性;
电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙中的一种.同学们经过讨论认为白色固体不可能是氧化钙,因为氧化钙会与水反应.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃 | 气体燃烧,产生黄色火焰并伴有浓烈黑烟 | 电石与水反应产生的气体是乙炔(C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸 | 固体溶解,没有气泡产生 | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后的固体于试管中加水,向上层清液中滴加酚酞 | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
| A. |  铁架台 | B. |  水槽 | C. |  坩锅钳 | D. |  表面皿 |
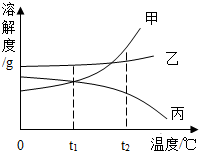 如图是甲、乙、丙三种物质的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液,请根据图中回答:
如图是甲、乙、丙三种物质的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液,请根据图中回答: