题目内容
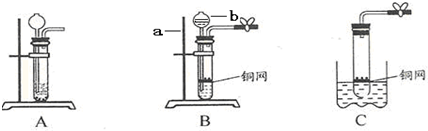
13.有一包白色粉末,可能含有碳酸钠、氢氧化钠、硝酸钡、氯化钠、硫酸铜、氯化铵一种或几种.某兴趣小组为确定它们的组成设计并进行了如下实验:Ⅰ.取少量该白色粉末于试管中,加少量熟石灰并加热,没有明显现象.
Ⅱ.另取少量该白色粉末于试管中,加入足量的水溶解、过滤.得到白色滤渣和无色滤液.
Ⅲ.向Ⅱ中无色滤液中滴加无色酚酞试液.溶液变红;再加入过量稀盐酸,溶液由红色变成无色,并有气泡产生.
(1)由实验Ⅰ、Ⅱ、Ⅲ中的现象可推断出白色粉末甲中一定含有的物质是Na2CO3、Ba(NO3)2(写化学式,下同),一定不含有的物质是(NH4)2Cl、CuSO4;
(2)写出步骤Ⅲ中一定发生反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(3)为了进一步探究白色粉末甲中可能含有的物质是否存在,兴趣小组继续进行了如下实验,结果证明了可能含有的物质确实存在.
Ⅳ.取步骤Ⅱ中的无色滤液少量,先加,再滴加硝酸银溶液,有白色沉淀产生.得出结论:其中一种物质确实存在.
Ⅴ.另取步骤Ⅱ中的无色滤液少量,先加,过滤,在滤液中滴加酚酞溶液,根据其现象得出另外一种物质确实存在的结论.
分析 铵盐和显碱性的物质在加热条件下反应能够产生氨气,氨气是一种有刺激性气味的气体;
溶液中的铜离子是蓝色的;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
氯化钠和硝酸银反应生成白色沉淀氯化银和硝酸钠;
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
氢氧化钠溶液显碱性,能使酚酞试液变红色.
解答 解:Ⅰ.取少量该白色粉末于试管中,加少量熟石灰并加热,没有明显现象,说明固体中不含有氯化铵;
Ⅱ.另取少量该白色粉末于试管中,加入足量的水溶解、过滤,得到白色滤渣和无色滤液,说明固体中含有碳酸钠和硝酸钡,不含有硫酸铜;
(1)由实验Ⅰ、Ⅱ、Ⅲ中的现象可推断出白色粉末甲中一定含有的物质是Na2CO3、Ba(NO3)2,一定不含有的物质是 (NH4)2Cl、CuSO4.
故填:Na2CO3、Ba(NO3)2; (NH4)2Cl、CuSO4.
(2)步骤Ⅲ中一定发生反应的是碳酸钠和稀盐酸反应生成了氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)Ⅳ.取步骤Ⅱ中的无色滤液少量,先加稀硝酸,再滴加硝酸银溶液,有白色沉淀产生,白色沉淀是氯化钠和硝酸银反应生成的氯化银,因此固体中含有氯化钠;
Ⅴ.另取步骤Ⅱ中的无色滤液少量,先加足量的氯化钙溶液,过滤,在滤液中滴加酚酞试液,酚酞试液变红色,说明固体中含有氢氧化钠.
故填:酚酞.
点评 有一包白色粉末,可能含有碳酸钠、氢氧化钠、硝酸钡、氯化钠、硫酸铜、氯化铵一种或几种.某兴趣小组为确定它们的组成设计并进行了如下实验:

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
4. 用“
用“ ”和“
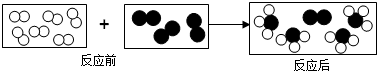
”和“ ”代表两种不同的分子,它们在一定条件下能发生变化,变化前后的模拟模型如下图所示,下列说法正确的是( )
”代表两种不同的分子,它们在一定条件下能发生变化,变化前后的模拟模型如下图所示,下列说法正确的是( )
 用“
用“ ”和“
”和“ ”代表两种不同的分子,它们在一定条件下能发生变化,变化前后的模拟模型如下图所示,下列说法正确的是( )
”代表两种不同的分子,它们在一定条件下能发生变化,变化前后的模拟模型如下图所示,下列说法正确的是( )| A. | 分子是化学变化中的最小粒子 | |
| B. | 该反应有2种生成物 | |
| C. | 参加反应的“ ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| D. | 该反应是化合反应 |
8.正确进行化学实验操作十分重要,下列图示实验操作中正确的是( )
| A. |  读出液体体积 | B. |  过滤 | C. |  熄灭酒精灯 | D. |  取固体药品 |
18.下列能说明镁带燃烧发生的是化学变化的是( )
| A. | 发出耀眼的白光 | B. | 放出热量 | ||
| C. | 生成一种白色的固体 | D. | 无法确定 |
3.某同学在测定某未知蓝色溶液的组成时,得出了以下结论.其中正确的是( )
| A. | KCl CuSO4 NaOH HCl | B. | CuCl2 NaCl BaCl2 KNO3 | ||
| C. | CuSO4 HCl BaCl2 NaNO3 | D. | NaCl KNO3 HNO3 Na2SO4 |