题目内容
根据如图所示制取气体的装置,回答下列问题(装置选择用序号填写):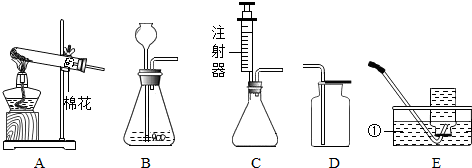
(1)实验仪器①的名称是 .
(2)用高锰酸钾制取氧气时,反应的化学方程式为 ,所选用的发生装置是 ,若收集干燥的氧气应选用的装置是 ,验满的方法是 .
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是 .
(4)用大理石和稀盐酸制取二氧化碳时,反应的化学方程式为 .若装置B中反应剧烈,从实验安全角度考虑,不宜采取的措施有 (填序号).
①用容积较小的锥形瓶;②减慢液体的滴加速度;③加热反应物;④降低液体反应物的浓度.

(1)实验仪器①的名称是
(2)用高锰酸钾制取氧气时,反应的化学方程式为
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是
(4)用大理石和稀盐酸制取二氧化碳时,反应的化学方程式为
①用容积较小的锥形瓶;②减慢液体的滴加速度;③加热反应物;④降低液体反应物的浓度.
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,氧气的检验和验满,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)依据仪器图示及其作用,辨识常用仪器,正确写出仪器名称;
(2)根据实验室用高锰酸钾制取氧气,是固体的加热反应来选择反应装置;并根据反应物和反应条件写出化学反应式;然后根据氧气的密度大于空气的密度和要收集干燥氧气的条件,选择收集装置;根据氧气支持燃烧的性质解答;
(3)根据C装置的特点分析其优点;
(4)根据发生装置的选择条件进行分析,并据反应原理书写方程式,并根据影响反应速率的因素判断.
(2)根据实验室用高锰酸钾制取氧气,是固体的加热反应来选择反应装置;并根据反应物和反应条件写出化学反应式;然后根据氧气的密度大于空气的密度和要收集干燥氧气的条件,选择收集装置;根据氧气支持燃烧的性质解答;
(3)根据C装置的特点分析其优点;
(4)根据发生装置的选择条件进行分析,并据反应原理书写方程式,并根据影响反应速率的因素判断.
解答:解:
(1)仪器①水槽;
(2)实验室用高锰酸钾制取氧气,是固体的加热反应,所以我们可以用A作为发生装置;反应的方程式是:2KMnO4
K2MnO4+MnO2+O2↑;要收集干燥的气体可用排空气法收集,又因为氧气的密度大于空气的密度,我们可用向上排空气法收集,所以选D作为收集装置;氧气有助燃的作用,我们可以将带火星的小木条放在集气瓶口上方,复燃说明已满.
(3)装置适于固体和液体的反应,制取氧气可用过氧化氢液体和二氧化锰固体反应,C装置制取气体的优点是可以控制反应的发生与停止;
(4)用大理石和稀盐酸反应制取二氧化碳,不需加热,故选发生装置B,反应的方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;根据题目信息可知,要减缓反应速率,可减少反应物的量或降低液体反应物的浓度,而采用容积较小的锥形瓶,或加热反应物都不安全;
答案:
(1)水槽
(2)2KMnO4
K2MnO4+MnO2+O2↑ A D 将带火星的木条放在集气瓶口,木条复燃,则氧气已满.
(3)可以控制反应的速率
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑ ①③
(1)仪器①水槽;
(2)实验室用高锰酸钾制取氧气,是固体的加热反应,所以我们可以用A作为发生装置;反应的方程式是:2KMnO4
| ||
(3)装置适于固体和液体的反应,制取氧气可用过氧化氢液体和二氧化锰固体反应,C装置制取气体的优点是可以控制反应的发生与停止;
(4)用大理石和稀盐酸反应制取二氧化碳,不需加热,故选发生装置B,反应的方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;根据题目信息可知,要减缓反应速率,可减少反应物的量或降低液体反应物的浓度,而采用容积较小的锥形瓶,或加热反应物都不安全;
答案:
(1)水槽
(2)2KMnO4
| ||
(3)可以控制反应的速率
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑ ①③
点评:掌握实验室制取气体的方法和装置,应该根据反应物的状态和反应的条件选择合适的发生装置;根据制取气体的水溶性和密度与空气相比来选择收集气体的方法.

练习册系列答案
相关题目
甲、乙两种固体的溶解度曲线如图所示.下列说法中,不正确的是( )
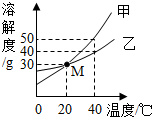

| A、M点表示在20℃时,甲、乙的溶解度相同 |
| B、40℃时,分别在100g水中加入50g甲、乙,充分搅拌,所得溶液中溶质的质量分数:甲大于乙 |
| C、40℃时,分别在100g水中加入35g甲、乙,充分搅拌并同时降温至20℃,析出固体的质量:甲大于乙 |
| D、20℃时,分别在50g水中加入40g甲、乙,充分搅拌并加热到40℃时,二者均为饱和溶液 |
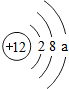 ,则a的值为
,则a的值为