题目内容
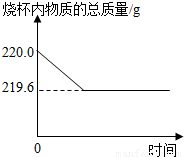
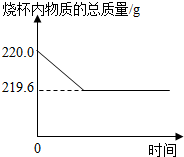
黄铜是一种重要的金属材料,我国约在南北朝就开始冶炼黄铜.黄铜是铜和锌的合金,它可以用来制造机器、电器零件及日常用品.准确称取20g黄铜屑样品放于盛有200g稀硫酸的烧杯中,恰好完全反应.测得烧杯内物质的总质量与时间的关系如图所示(气体溶解忽略不计).试计算:
(1)生成氢气的质量是______g;
(2)该黄铜屑样品中铜的质量分数?
(3)所用稀硫酸的溶质质量分数是多少?(写出计算过程)
【答案】分析:(1)依据质量守恒定律可以利用烧杯内物质的质量之差求出生成氢气的质量;
(2)根据氢气的质量利用方程式可以求出反应的锌的质量,从而可以求出黄铜屑样品中铜的质量分数;
(3)根据氢气的质量也可求出反应的稀硫酸的质量,进而求出所用稀硫酸的溶质质量分数;
解答:解:(1)黄铜中的铜不能与酸反应生成氢气,而锌能与稀硫酸反应生成氢气,依据质量守恒定律可以利用烧杯内物质的质量之差求出生成氢气的质量,利用图象数据可知其质量为220g-219.6g=0.4g;
(2)设反应的锌的质量是x,硫酸的质量是y
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.4g
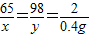
x=13g y=19.6g
故该黄铜屑样品中铜的质量分数为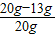 ×100%=35%
×100%=35%
(3)则所用稀硫酸的溶质质量分数是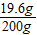 ×100%=9.8%
×100%=9.8%
故答案为:(1)0.4;(2)(2)该黄铜屑样品中铜的质量分数为35%;(3)所用稀硫酸的溶质质量分数是9.8%;
点评:本题难度不是很大,利用质量守恒定律由反应前后烧杯内物质的总质量的差计算出生成氢气的质量是解答本题的突破口.
(2)根据氢气的质量利用方程式可以求出反应的锌的质量,从而可以求出黄铜屑样品中铜的质量分数;
(3)根据氢气的质量也可求出反应的稀硫酸的质量,进而求出所用稀硫酸的溶质质量分数;
解答:解:(1)黄铜中的铜不能与酸反应生成氢气,而锌能与稀硫酸反应生成氢气,依据质量守恒定律可以利用烧杯内物质的质量之差求出生成氢气的质量,利用图象数据可知其质量为220g-219.6g=0.4g;
(2)设反应的锌的质量是x,硫酸的质量是y
Zn+H2SO4=ZnSO4+H2↑
65 98 2
x y 0.4g
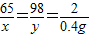
x=13g y=19.6g
故该黄铜屑样品中铜的质量分数为
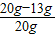 ×100%=35%
×100%=35%(3)则所用稀硫酸的溶质质量分数是
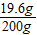 ×100%=9.8%
×100%=9.8%故答案为:(1)0.4;(2)(2)该黄铜屑样品中铜的质量分数为35%;(3)所用稀硫酸的溶质质量分数是9.8%;
点评:本题难度不是很大,利用质量守恒定律由反应前后烧杯内物质的总质量的差计算出生成氢气的质量是解答本题的突破口.

练习册系列答案
相关题目
 体溶解忽略不计).
体溶解忽略不计).