题目内容
某化工厂生产的碳酸钠产品中含有少量的氯化钠(其他杂质忽略不计),取一定量固体样品,放入烧杯中,加入137.7g水充分溶解,再向烧杯中加入溶质的质量分数为7.3%的稀盐酸300g恰好完全反应.待气体完全逸出后,测得所得溶液中溶质的质量分数为10%.计算样品中碳酸钠的质量分数.
解:盐酸中溶质质量为:300g×7.3%=21.9g,设与21.9g氯化氢反应需要碳酸钠的质量为X,生成氯化钠的质量为y,生成二氧化碳的质量为z则:
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x 21.9g y z
根据: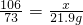 解得x=31.8g,根据:
解得x=31.8g,根据: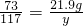 解得y=35.1g,根据:
解得y=35.1g,根据: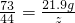 解得z=13.2g;
解得z=13.2g;
设原样品质量为k则: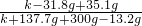 =10%,解得k=50.8g,所以样品中碳酸钠的质量分数:
=10%,解得k=50.8g,所以样品中碳酸钠的质量分数: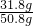 ×100%=62.3%
×100%=62.3%
故答案为:62.3%.
分析:根据盐酸的质量计算出参加反应的碳酸钠的质量,生成二氧化碳的质量,生成的氯化钠的质量,再根据所得溶液中溶质的质量分数为10%求出样品的质量,用碳酸钠的质量除以样品的质量,乘以百分之百即可.
点评:解答本题容易出错的地方是在计算最后所得溶液的溶质质量分数时,溶质有两部分:原来样品中氯化钠的质量和新生成的氯化钠的质量.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x 21.9g y z
根据:
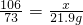 解得x=31.8g,根据:
解得x=31.8g,根据: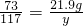 解得y=35.1g,根据:
解得y=35.1g,根据: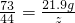 解得z=13.2g;
解得z=13.2g;设原样品质量为k则:
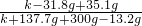 =10%,解得k=50.8g,所以样品中碳酸钠的质量分数:
=10%,解得k=50.8g,所以样品中碳酸钠的质量分数: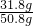 ×100%=62.3%
×100%=62.3%故答案为:62.3%.
分析:根据盐酸的质量计算出参加反应的碳酸钠的质量,生成二氧化碳的质量,生成的氯化钠的质量,再根据所得溶液中溶质的质量分数为10%求出样品的质量,用碳酸钠的质量除以样品的质量,乘以百分之百即可.
点评:解答本题容易出错的地方是在计算最后所得溶液的溶质质量分数时,溶质有两部分:原来样品中氯化钠的质量和新生成的氯化钠的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目