题目内容
3.在实验室中可选择如图装置制取气体.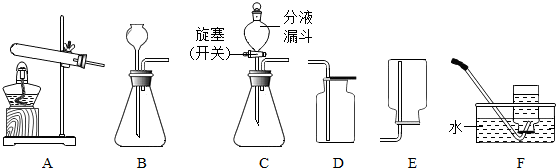
(1)若选择A、F组合一套装置制取了某气体,请写出有关反应的化学方程式.2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)制取CO2的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;其发生装置可选择B或C,与B相比较,C的主要优点是什么?
(3)若用金属与酸反应来制取氢气,应选择以上哪些装置?(写出一套发生和收集装置即可)BE或BF或CE或CF.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.C的主要优点是:可以控制反应的速度.
解答 解:(1)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;C的主要优点是:可以控制反应的速度;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;可以控制反应的速度;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,发生装置选B或C,收集装置选E或F;故答案为:BE或BF或CE或CF.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列实验操作中,正确的是( )
| A. |  检查装置气密性 | B. |  除去CO中水蒸气 | C. |  测定溶液pH | D. |  稀释浓硫酸 |
11.物质甲是一种重要的化工原料,在点燃条件下可以和乙反应生成丙和丁.根据如图所示微观示意图得出的结论中,正确的是( )


| A. | 乙、丙、丁都是氧化物 | B. | 反应前后分子总数不变 | ||
| C. | 该反应是吸热反应 | D. | 反应中乙和丁的质量比是24:9 |
18.下列认识或说法中,正确的是( )
| A. | 向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- | |
| B. | 常温下可用Fe与AgCl反应制取Ag | |
| C. | 可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| D. | 将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色 |
12.下列成语中蕴含化学变化的是( )
| A. | 百炼成钢 | B. | 花香四溢 | C. | 滴水成冰 | D. | 扬汤止沸 |
13.下列说法不正确的是( )
| A. | 蒸发食盐水,当蒸发皿中出现较多固体时,停止加热 | |
| B. | 配制100g20%的氯化钠溶液,需要氯化钠20g | |
| C. | 溶解过程中用玻璃棒搅拌的作用是加速溶解 | |
| D. | 从100mL 20%的食盐水中取出50mL,剩余溶液的溶质质量分数为10% |





