��Ŀ����
��������������������������أ�
��1����ͼ1Ϊ�����ڿ����е����������������������IJ�λ����������ֹ�˵�����ɲ�ȡ�Ĵ�ʩ��������
��2����ͼ2ΪԪ�����ڱ��е�һ������˵������ȷ����������
A�����ǵؿ��к������Ľ���Ԫ�� B����ԭ�ӵĺ��������Ϊ13
C����Ԫ�ص�ԭ�ӽṹʾ��ͼΪͼ3 D����Ԫ�ص����ԭ������Ϊ26.98
��3�����о���������ʱ��ijС��ͬѧ����������ʵ��̽����
��һ�������ۼ��뵽����п������ͭ�Ļ����Һ�У���ַ�Ӧ����ˣ�Ȼ�����ֽ�ϵ����ʽ��з�����ʵ�飮
��������⡿��ֽ�ϵ�������ʲô��
���������롿����Ϊֻ��ͭ������Ϊ��ͭ�����Ļ�������Ϊ��ͭ������п�Ļ���
���������ۡ����һ����Ϊ���IJ��벻��������������������
��ʵ������ۡ�ͬѧ��ͨ��ʵ��ȷ������ֽ�����ʵijɷ֣�����д���пհף�
| ʵ�鲽�� | ����ͽ��� | �йط�Ӧ�Ļ�ѧ����ʽ |
| ȡ������ֽ��ʣ������ʣ�����������������Һ | ���� | ���� |
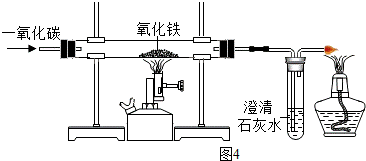
��4����������������������зdz���Ҫ�IJ��ϣ���ʵ���ҳ�ȡ20g��������Ʒ���ڲ���������ͼ4���Ƶ���Ʒ�Ͳ����ܵ�������Ϊ70g��ͨ������CO�����ʹ��Ʒ��ַ�Ӧ�����ʲ��μӷ�Ӧ������ȴ��Ƶò����ܺ�ʣ������������Ϊ65.2g���Լ�����Ʒ��Fe2O3������������
| ������ʴ���������������ʵ��̽�����ʵ����ʻ�仯���ɣ������Ļ�ѧ���ʣ�Ԫ�����ڱ����ص㼰��Ӧ�ã����ݻ�ѧ��Ӧ����ʽ�ļ��㣮 | |
| ר�⣺ | ������������ϣ� |
| ������ | ��1������ˮ������ͬʱ�Ӵ�ʱ�������⣬��˸���ˮ���������Է�ֹ����Ʒ���⣻ ��2��ԭ���У��������������ں���������� ��3��п�������ã�����ͭ���ã��Ƚϻ��õĽ����ܹ��Ѳ����õĽ�������������Һ���û������� ��4�����ݷ�Ӧǰ�����������Լ�������������Ԫ�ص���������һ�����Լ������������������Ӷ����Լ�����Ʒ��Fe2O3������������ |
| ��� | �⣺��1��B��������ˮ��������ֽӴ������������⣻ �������ɣ�Ϳ��ʳ���ͣ����Է�ֹ�˵����⣮ ���B���������ɣ�Ϳ��ʳ���ͣ� ��2��A�����ǵؿ��к������Ľ���Ԫ�أ���ѡ��˵����ȷ�� B����ԭ�ӵĺ��������Ϊ13����ѡ��˵����ȷ�� C����Ԫ�ص�ԭ�ӽṹʾ��ͼ�У�Ӧ����3�����Ӳ㣬���е�3����3�����ӣ���ѡ��˵������ȷ�� D����Ԫ�ص����ԭ������Ϊ26.98����ѡ��˵����ȷ�� ���C�� ��3�����һ����Ϊ���IJ��벻��������Ϊп�������ã��������û�����п�е�п��������ֽ��û��п�� ȡ������ֽ��ʣ������ʣ�����������ϡ���ᣬ���������ݣ����Ҳ�����ȷ�������������ݣ���ײ�����ȷ�� ����ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Fe+2HCl�TFeCl2+H2���� ���п�������ã��������û�����п�е�п��ϡ������������ݣ����Ҳ�����ȷ�������������ݣ���ײ�����ȷ��Fe+2HCl�TFeCl2+H2���� ��4������������Ԫ�ص�����Ϊ��70g��65.2g=4.8g�� ��������������Ϊx�����У�x�� x=16g�� ����Ʒ��Fe2O3����������Ϊ�� ����Ʒ��Fe2O3����������Ϊ80%�� |
| ������ | ���⿼������������������ֹ����ķ�����ԭ�ӽṹʾ��ͼ���йط���ļ���ȷ����֪ʶ������ʱҪע��淶�Ժ�ȷ�ԣ� |

 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д��������и������ʣ����õ����ַ�������ȷ���ǣ�������
| ѡ�� | �����ֵ����� | ����һ | ������ |
| A | ̼������Һ��̼��������Һ | �����̪��Һ | ����ϡ���� |
| B | ��ͭ�ͻƽ� | ��������ͭ��Һ | �ڿ����м��� |
| C | ʯ��ˮ������������Һ | ͨ�������̼���� | ������ɫʯ����Һ |
| D | ��ʯ�Һ���ʯ�� | ��ˮ�۲� | ��ˮ��ֱ�����̪��Һ |
| �� | A�� | A | B�� | B | C�� | C | D�� | D |
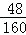 ��100%=4.8g��
��100%=4.8g��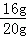 ��100%=80%��
��100%=80%�� C6H1206+6O2����X�Ļ�ѧʽΪ������
C6H1206+6O2����X�Ļ�ѧʽΪ������ CaO+B��
CaO+B��  B��ȷ��B������������˵��D���ʵ�һ����ѧ���ʣ�������
B��ȷ��B������������˵��D���ʵ�һ����ѧ���ʣ�������