题目内容
17.用工业碳酸钙(含有少量Al2O3、Fe2O3)生产医药CaCl2•2H2O的主要流程如下:
(1)加入试剂A的目的是除去溶液1中少量AlCl3、FeCl3.试剂A可以选择c(选填序号).
a.Na2CO3 b.Ba(OH)2 c.Ca(OH)2
(2)阶段一的目的是除去工业碳酸钙中的杂质.
(3)操作1、2中,所用玻璃仪器有漏斗、玻璃棒、烧杯、胶头滴管.操作3包括:蒸发浓缩、降温结晶、过滤、洗涤等.
分析 (1)根据氢氧根离子和铝离子、铁离子反应会生成沉淀,钙离子不会引入新的杂质进行分析;
(2)根据阶段一可以除去碳酸钙中的氧化铝、氧化铁等杂质进行分析;
(3)根据过滤需要的仪器,溶液结晶的过程进行分析.
解答 解:(1)除去铝离子、铁离子常用氢氧根离子,钡离子会引入新的杂质,所以应选择氢氧化钙,故选:c;
(2)阶段一可以除去碳酸钙中的氧化铝、氧化铁等杂质,所以阶段一的目的是:除去工业碳酸钙中的杂质;
(3)通过分析可知,操作1、2是过滤,过滤需要的仪器有烧杯、漏斗、玻璃棒、胶头滴管,操作3是从溶液中得到固体,包括:蒸发浓缩、降温结晶、过滤、洗涤等.
故答案为:(1)c;
(2)除去工业碳酸钙中的杂质;
(3)漏斗,降温结晶.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

练习册系列答案
相关题目
7.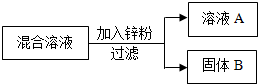 工厂废水中含有硝酸银和硝酸铜,为了回收其中的铜和银,进行了如图所示实验,并对溶液A和固体B的成分进行了分析和实验探究.
工厂废水中含有硝酸银和硝酸铜,为了回收其中的铜和银,进行了如图所示实验,并对溶液A和固体B的成分进行了分析和实验探究.
【提出问题】溶液A中的溶质可能有哪些?
【做出猜想】①只有硝酸锌 ②硝酸锌、硝酸银 ③硝酸锌、硝酸铜 ④硝酸锌、硝酸铜、硝酸银
【交流讨论】不合理的猜想是②(填序号),理由是猜想②中无Cu(NO3)2,说明已与Zn反应生成Cu,而Cu能与AgNO3反应,不可能有AgNO3.
【实验探究】若猜想①成立,通过以下实验可探究固体B的成分,请填写此表.
 工厂废水中含有硝酸银和硝酸铜,为了回收其中的铜和银,进行了如图所示实验,并对溶液A和固体B的成分进行了分析和实验探究.
工厂废水中含有硝酸银和硝酸铜,为了回收其中的铜和银,进行了如图所示实验,并对溶液A和固体B的成分进行了分析和实验探究.【提出问题】溶液A中的溶质可能有哪些?
【做出猜想】①只有硝酸锌 ②硝酸锌、硝酸银 ③硝酸锌、硝酸铜 ④硝酸锌、硝酸铜、硝酸银
【交流讨论】不合理的猜想是②(填序号),理由是猜想②中无Cu(NO3)2,说明已与Zn反应生成Cu,而Cu能与AgNO3反应,不可能有AgNO3.
【实验探究】若猜想①成立,通过以下实验可探究固体B的成分,请填写此表.
| 实验步骤 | 实验现象 | 化学方程式及结论 |
| 取少量固体B,滴加稀盐酸(或稀硫酸等) | 有气泡产生 | Zn+2HCl=ZnCl2+H2↑或(Zn+H2SO4=ZnSO4+H2↑) 固体B的成分是Zn、Cu、Ag |
5.下列指定反应的化学方程式正确的是( )
| A. | 铁丝在氧气中燃烧:4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 铝片溶于稀硫酸:Al+H2SO4═AlSO4+H2↑ | |
| C. | 铜绿的形成:2Cu+O2+H2O+CO2═Cu2(OH)2CO3 | |
| D. | 过氧化钠与二氧化碳反应生成纯碱和氧气:Na2O2+CO2═Na2CO3+O2 |
12.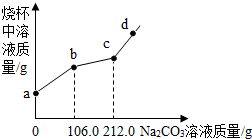 烧杯中盛有BaCl2和HCl液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有BaCl2和HCl液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
 烧杯中盛有BaCl2和HCl液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有BaCl2和HCl液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )| A. | ab段产生白色沉淀 | |
| B. | bc段溶液质量增加86.3g | |
| C. | c点对应溶液的溶质质量分数为7.5% | |
| D. | 向d点溶液中滴加酚酞试液,溶液显红色 |
2.下列关于水的物理性质的描述正确的是( )
| A. | 水是无色无味的液体 | B. | 水的沸点是100℃ | ||
| C. | 水的熔点是0℃ | D. | 水的导电能力很差 |
4. 如图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,你认为下列说法正确的是( )
如图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,你认为下列说法正确的是( )
 如图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,你认为下列说法正确的是( )
如图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,你认为下列说法正确的是( )| A. | 该反应属于化合反应 | |
| B. | 分子在化学变化中不可分 | |
| C. | 化学反应前后元素的种类发生了变化 | |
| D. | 生成物一定是混合物 |
1.空气中含量最多且化学性质不活泼的气体是( )
| A. | O2 | B. | N2 | C. | CO2 | D. | 稀有气体 |
2.室温下,把CaCl2 的饱和溶液和蒸馏水区别开来,下列方法中不可行的是( )
| A. | 加肥皂水 | B. | 测导电性 | ||
| C. | 分别通二氧化碳看是否有沉淀 | D. | 降温至0℃看是否凝固 |