题目内容
4.通过煅烧MnSO4•H2O可制得MnxO4,如图是煅烧MnSO4•H2O时温度与剩余固体质量变化曲线.下列分析正确的是( )
| A. | 曲线中A段表示的物质是Mn2(SO4)3 | B. | 曲线A段表示的物质是MnO2 | ||
| C. | MnxO4中x=3 | D. | MnxO4中x=5 |
分析 根据MnSO4•H2O在高温下易分解,产物是MnxO4、含硫化合物、水,依据固体质量-分解温度的关系图象,分析质量变化与对应的化学反应,求解A段所表示物质的化学式和x的值解答.
解答 解:
探究物质的变化规律时,运用了物质的质量守恒和元素的质量守恒法.MnSO4•H2O在高温下易分解,101.4克的MnSO4•H2O物质的量为:$\frac{101.4g}{169g/mol}$=0.6mol,根据锰元素守恒,MnSO4•H2O分解时,先转变为MnSO4和H2O,质量为:0.6mol×151g/mol=90.60g,所以图2曲线中A段质量减少:101.4-90.60=10.8克为水,所以该曲线中A段所表示物质的化学式为MnSO4,根据表中的数据可知:B固体质量为45.80克,为MnxO4,根据锰元素守恒,MnxO4的物质的量为$\frac{0.6}{x}$mol,则$\frac{0.6}{x}$mol×(55x+16×4)g/mol=45.80g,x=3,
A.曲线中A段表示的物质是MnSO4,故正确;
B、曲线中A段表示的物质是MnSO4,不是MnO2;故错误;
C、MnxO4中x=3,故正确;
D、MnxO4中x=3,不是x=5,故错误.
答案:C.
点评 本题难度较大,根据锰元素守恒是解答的关键.

练习册系列答案
相关题目
16.下列除杂(括号内是杂质)所选试剂合理的是( )
| A. | Cu(Fe) 稀盐酸 | B. | CO2气体(HCl) 氢氧化钠溶液 | ||
| C. | CuO(Cu) 稀硫酸 | D. | Na2SO4溶液(Na2CO3) 氯化钡溶液 |

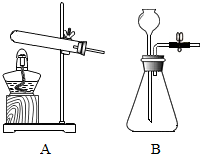 如图是实验室常用的气体发生装置,请回答有关问题.
如图是实验室常用的气体发生装置,请回答有关问题.