题目内容
在测定空气中氧气含量的试验中,不能证明的是( )
| A、氮气不易溶于水 | ||
| B、氧气能与红磷反应 | ||
| C、氮气的密度比空气大 | ||
D、氧气约占空气体积的
|
考点:空气组成的测定
专题:空气与水
分析:红磷燃烧生成五氧化二磷,消耗氧气后,根据进入集气瓶中的水的量,可以判断氧气的体积分数.
解答:解:在测定空气中氧气含量的试验中,可以证明氧气能和红磷反应,通过进入集气瓶中的水的量可以判断氧气约占空气总体积的五分之一,同时证明氮气不溶于水,不能燃烧,不支持燃烧;不能证明氮气的密度比空气大.
故选:C.
故选:C.
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
将Na2CO3?10H2O与NaHCO3的混合物m g溶解于水配制成100mL溶液,测知m(Na+)=0.92g,若将溶液蒸干灼烧直至质量不变,可得固体( )
| A、2.12 g |
| B、2.55 g |
| C、1.86 g |
| D、无法确定 |
下列变化中,属于物理变化且对其解释正确的是( )
| A、二氧化碳气体制成干冰体积变小,是因为二氧化碳分子变小了 |
| B、水结冰体积变大,是因为水的密度比冰的大 |
| C、碳酸钠晶体在干燥空气里变成粉末,是因为在干燥空气里碳酸钠晶体易失去结晶水 |
| D、活性炭吸附有毒气体,是因为活性炭与有毒气体发生了反应 |
下列药品保存和实验基本操作正确的是 ( )
A、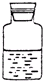 保存NaOH溶液 |
B、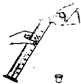 倾倒液体 |
C、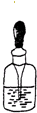 滴瓶的滴管用后直接插回原瓶 |
D、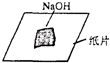 称量NaOH固体 |
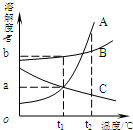 如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列说法错误的是( )
如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列说法错误的是( )| A、t1℃时,三种物质中B的溶解度最大 |
| B、t2℃时,取三种物质各a g分别放入100g水中充分溶解,只有C物质能形成饱和溶液 |
| C、将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,所得溶液的溶质质量分数大小关系为:B>A=C |
| D、可用降温的方法使接近饱和的C溶液变为饱和溶液 |
下列各组内的两种微粒所含质子数和电子数都相同的是( )
| A、Cl- 和 Ca2+ |
| B、Mg2+和Mg |
| C、HF 和 NH3 |
| D、H2O和 Na+ |
锌粉、铝粉、铁粉、镁粉的混合物3.8克与一定质量的稀硫酸恰好完全反应,将反应后的混合物蒸发水分得固体13.4克,则生成氢气的质量为( )
| A、0.2克 | B、9.6克 |
| C、9.8克 | D、0.18克 |