题目内容
9.家用清洁产品中蕴含着丰富的化学知识.根据下表回答问题.| 清洁产品 | 除垢净 | 去污粉 | 管道通 |
| 主要成分 | 盐酸 | 碳酸钠 | 氢氧化钠、铝粉 |
(2)去污粉与除垢净不能混合使用,其原因是Na2CO3+2HCl═2NaCl+H2O+CO2↑(用化学方程式表示).
(3)管道通使用时不能接触皮肤是因为氢氧化钠具有较强的腐蚀性.
分析 (1)根据除垢净的主要成分是盐酸,能与铁反应生成氯化亚铁溶液和氢气,进行分析解答.
(2)根据去污粉的主要成分碳酸钠能与除垢净的主要成分是盐酸反应,生成氯化钠、水和二氧化碳,进行分析解答.
(3)根据管道通的主要成分之一是氢氧化钠,进行分析解答.
解答 解:(1)除垢净的主要成分是盐酸,能与铁反应生成氯化亚铁溶液和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
(2)去污粉的主要成分碳酸钠能与除垢净的主要成分是盐酸反应,生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)管道通的主要成分之一是氢氧化钠,氢氧化钠具有强烈的腐蚀性,管道通使用时不能接触皮肤.
故答案为:(1)Fe+2HCl═FeCl2+H2↑;(2)Na2CO3+2HCl═2NaCl+H2O+CO2↑;(3)氢氧化钠具有较强的腐蚀性.
点评 本题难度不大,掌握碳酸钠的化学性质、酸的化学性质、氢氧化钠具有强烈的腐蚀性是正确解答本题的关键.

练习册系列答案
相关题目
20.下列实验操作正确的是( )
| A. |  CO2验满 | B. | 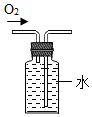 收集O2 | C. | 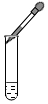 滴加液体 | D. | 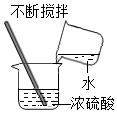 稀释浓硫酸 |
4.将下列固体分别放入水中,溶液温度明显降低的是( )
| A. | 硝酸铵 | B. | 生石灰 | C. | 烧碱 | D. | 氯化钠 |
1.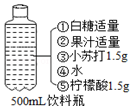 厨房中的实验室
厨房中的实验室
(1)在厨房中可以自制碳酸饮料,配料表如图所示.产生的二氧化碳气体是配料表中的柠檬酸与小苏打反应生成的,人体胃液中的酸也可以与该物质反应,其方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(2)紫罗兰的花瓣汁液呈紫色,将它分别滴加到盛有下列溶液的试管中有如下现象:
将紫罗兰花瓣汁液滴入肥皂水中溶液呈蓝色,说明肥皂水显碱性.
 厨房中的实验室
厨房中的实验室(1)在厨房中可以自制碳酸饮料,配料表如图所示.产生的二氧化碳气体是配料表中的柠檬酸与小苏打反应生成的,人体胃液中的酸也可以与该物质反应,其方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(2)紫罗兰的花瓣汁液呈紫色,将它分别滴加到盛有下列溶液的试管中有如下现象:
| 溶液名称 | 白醋 | 稀盐酸 | 氯化钠溶液 | 蒸馏水 | 石灰水 | 氢氧化钠溶液 |
| 紫罗兰 | 红色 | 红色 | 紫色 | 紫色 | 蓝色 | 蓝色 |
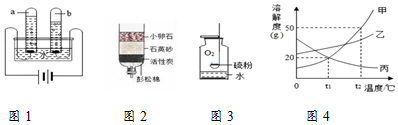
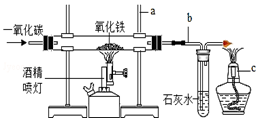 实验室模拟炼铁的实验装置如图所示.
实验室模拟炼铁的实验装置如图所示.