题目内容
14.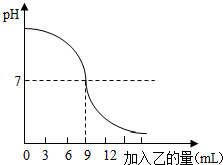 已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,请分析曲线回答问题:
已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,请分析曲线回答问题:①甲是氢氧化钠溶液;
②当加入乙溶液的体积为9ML,甲、乙溶液恰好完全反应;
③当加入的盐酸为6mL时,溶液中的溶质是氯化钠和氢氧化钠;
④溶液中的溶质是NaCl,NaOH时,溶质的pH为大于7.
分析 ①根据图象中pH值的变化是从大于7逐渐的减小到小于7,即可确定操作的过程.
②氢氧化钠与稀盐酸反应生成氯化钠和水,甲、乙溶液恰好完全反应时,溶液显中性,进行分析解答.
③当加入的盐酸为6mL时,溶液的pH大于7,进行分析解答.
④溶液中的溶质是NaCl、NaOH时,溶液显碱性,进行分析解答.
解答 解:①由图象可知,pH值是开始时大于7逐渐的减小到7然后小于7,可知原溶液显碱性,然后不断的加入酸性溶液,使pH减小,说明是把稀盐酸滴加到氢氧化钠溶液中;则甲溶液为氢氧化钠溶液.
②氢氧化钠与稀盐酸反应生成氯化钠和水,甲、乙溶液恰好完全反应时,溶液显中性,溶液的pH=7,即当加入乙溶液的体积为9mL时,甲、乙溶液恰好完全反应.
③当加入的盐酸为6mL时,溶液的pH大于7,说明氢氧化钠溶液过量,溶液中的溶质是氯化钠和氢氧化钠.
④溶液中的溶质是NaCl、NaOH时,溶液显碱性,溶质的pH为大于7.
故答案为:①氢氧化钠;②9;③氯化钠和氢氧化钠;④大于7.
点评 本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
相关题目
2.以下粗盐提纯的操作步骤中,不需要使用玻璃棒的是( )
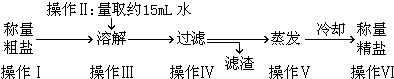

| A. | 操作Ⅱ:量取15mL水 | B. | 操作Ⅲ:粗盐溶解 | ||
| C. | 操作Ⅳ:过滤除去杂质 | D. | 操作Ⅴ:蒸发结晶 |
19.下列实验现象描述正确的是( )
| A. | 红磷在空气中燃烧产生大量白色烟雾 | |
| B. | 将打磨过的铝丝插入硫酸铜溶液中,银白色的铝丝表面覆盖一层红色固体 | |
| C. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体,放出大量的热 | |
| D. | 用稀盐酸除铁锈,溶液由无色变为浅绿色 |
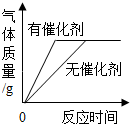
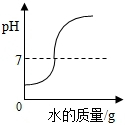
6.下列四个图象中,能正确反映其对应变化关系的是( )
 |  |  |  |
| A | B | C | D |
| A. | 分别用等质量、等质量分数的过氧化氢溶液制取氧气 | |
| B. | 向一定量的稀盐酸中加入足量的水稀释 | |
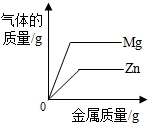
| C. | 向等质量、等质量分数的稀盐酸中分别逐渐加入锌粉、镁粉至过量 | |
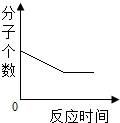
| D. | 在密闭容器中点燃H2和O2的混合气体 |
2.实验室可以用加热高锰酸钾制取氧气,生成锰酸钾、二氧化锰和氧气,其中锰酸钾(K2MnO4)中的Mn元素的化合价是( )
| A. | +4 | B. | +6 | C. | +7 | D. | -3 |
 水是重要资源.
水是重要资源.