题目内容
 食盐是我们生活中必不可少的调味品之一,其主要成分的化学式为NaCl.
食盐是我们生活中必不可少的调味品之一,其主要成分的化学式为NaCl.(1)已知在NaCl中氯元素的化合价为-1价,则钠元素的化合价为
(2)如图所示,20℃时食盐的溶解度是36g,这表明20℃时,在
(3)欲从海水中提取食盐,应采取的方法是
①蒸发海水使食盐结晶 ②冷却海水使食盐结晶.
考点:氯化钠与粗盐提纯,结晶的原理、方法及其应用,固体溶解度的概念,有关元素化合价的计算
专题:常见的盐 化学肥料
分析:(1)根据在化合物中正负化合价代数和为零,结合NaCl的化学式进行解.
(2)溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量,据此进行分析解答.
(3)冷却热饱和溶液结晶(降温结晶)一般适用于溶解度随温度变化较大的物质,如硝酸钾;蒸发溶剂结晶一般适用于溶解度随温度变化不大的物质,如食盐.
(2)溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量,据此进行分析解答.
(3)冷却热饱和溶液结晶(降温结晶)一般适用于溶解度随温度变化较大的物质,如硝酸钾;蒸发溶剂结晶一般适用于溶解度随温度变化不大的物质,如食盐.
解答:解:(1)在NaCl中氯元素的化合价为-1价,设钠元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-1)=0,则x=+1价.
(2)20℃时食盐的溶解度是36g,这表明20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态.
(3)食盐的溶解度受温度的影响变化不大,欲从海水中提取食盐,应采取的方法是蒸发海水使食盐结晶.
故答案为:(1)+1价;(2)100;(3)①.
(2)20℃时食盐的溶解度是36g,这表明20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态.
(3)食盐的溶解度受温度的影响变化不大,欲从海水中提取食盐,应采取的方法是蒸发海水使食盐结晶.
故答案为:(1)+1价;(2)100;(3)①.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、溶解度的含义、结晶的原理等是正确解答本题的关键.

练习册系列答案
相关题目
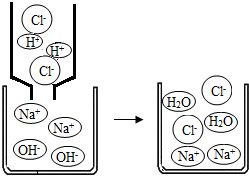 如图是盐酸与氢氧化钠溶液反应的微观过程示意图.构成氢氧化钠溶液的粒子是
如图是盐酸与氢氧化钠溶液反应的微观过程示意图.构成氢氧化钠溶液的粒子是
 按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题: