题目内容
向盛有AgNO3、Zn(NO3)2和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。根据上述现象,下列结论正确的是
A. 滤渣中一定有Fe、Zn B. 滤渣中可能有Ag、Cu
C. 滤液中一定有Fe(NO3) 2、Zn(NO3) 2 D. 滤液中可能有AgNO3、Cu(NO3) 2
C 【解析】充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,此现象说明Fe过量没有反应完,所以原混合溶液中的Cu(NO3)2、AgNO3全部被置换生成Cu、Ag和Fe(NO3)2溶液。则: A、铁的活动性比锌弱,不会置换出硝酸锌中的锌,错误; B、向滤渣中加入稀盐酸,有气泡产生,说明铁过量,所以滤渣中一定有Ag、Cu和Fe,错误;C、铁会与原混合溶液中的Cu(NO3)2、AgNO3全部... 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案王明觉得你很聪明,是他的良师益友,学完“酸的化学性质”后,邀请你与他讨论“食醋在厨房中的妙用”:
(1)复习酸的化学性质
①酸与指示剂作用 | 酸溶液能使紫色石蕊溶液变红色 | 酸溶液不能使无色酚酞溶液变色 |
②酸与活泼金属作用 | Fe+2HCl=FeCl2+H2↑ | Fe+H2SO4=FeSO4+H2↑ |
③酸与某些金属氧化物作用 | Fe2O3+HCl=FeCl2+H2O | …… |
④酸与碱作用 | ||
...... |
由于王明的课堂笔记没做好,“③酸与某些金属氧化物作用”后面的化学方程式书写错误,请帮他写出正确的化学方程式:_______________________________。
(2)讨论交流
(Ⅰ)王明自豪地说,目前世界卫生组织正在推广使用中国铁锅,使用铁锅炒菜时,放点食醋时,可以补充人体需要的微量元素______元素,该反应的原理是利用了酸的化学性质_________(填序号“①”、“②”或“③”)。铁与的稀盐酸反应后,溶液中的溶质可能含有HCl,下列物质能证明是___________
A.CuO B.AgNO3溶液 C.Cu D.NaOH溶液
(Ⅱ)你告诉王明,他总结的酸的化学性质④酸与碱作用,这类化学反应的基本反应类型是____________ 。
(3)反思
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都含有_______。(填符号)
Fe2O3+6HCl=2FeCl3+3H2O 铁 ② A 复分解反应 H+ 【解析】本题主要考查酸的化学性质及具有相似化学性质的原因。 (1)复习酸的化学性质:氧化铁与盐酸发生复分解反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl=2FeCl3+3H2O; (2)(Ⅰ) ①推广使用中国铁锅,使用铁锅炒菜时能补充人体需要的微量元素铁元素;该反应的原理是利用了酸与活泼金属...下图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点。
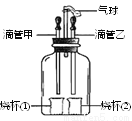
⑴ 若甲中吸有浓氨水,乙中吸有无色酚酞试液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞试液变红,说明分子具有的性质是_____________。
⑵ 若先将甲中的液体挤出,观察出气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起,过一会,略缩小,但不会恢复到原状。请将下表中的试剂补充完整。
滴管甲 | 烧杯① | 滴管乙 | 烧杯② | |
试剂 | H2O | ________ | _________ | Mg |
图示气球鼓起是因为装置内气压增大,第二次气压增大的原因是______________。
⑶ 若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末。为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应进行的实验操作是___________。
分子在不断的运动 氢氧化钠固体 稀盐酸 镁和盐酸反应生成气体且放热 先捏滴管乙,再捏滴管甲 【解析】(1)由于氨水和酚酞试液不在一个烧杯中,但酚酞试液变红了,说明氨水进入了酚酞试液中,氨水显碱性能使酚酞试液变红,所以说明了氨分子在不断运动,才运动到酚酞试液中的,所以说明分子在不断运动; (2)将甲中的液体挤出,观察到气球明显鼓起,由于甲中滴管是水,所以该物质溶于水放出热量,溶于水放热的...


