题目内容
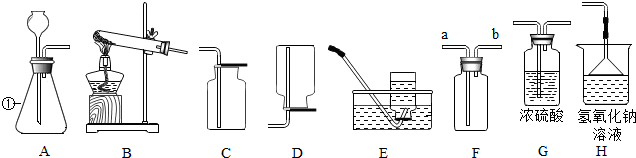
12.(1)实验室常利用以下装置完成气体制备及性质实验1,请回答:
①若用氯酸钾制取氧气,应选择的发生装置是A(填字母),实验过程中发现产生氧气和速率很慢,经检查不是氯酸钾变质,也不是装置气密性不好,你你认为可能的原因是未加二氧化锰;若用BC装置制取氧气,B中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②F是一种可用于集气、洗气等的多功能装置,若将F装置内装满水,再连接量筒,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从b(填“a”或“b”)进入F中.
③SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨,实验室用常用F装置来收集它,现利用如图2装置收集一瓶干燥的SO2气体,装置的导管按气流方向连接的顺序是d→c→a→b→e(填字母),装置的H的作用是吸收多余的SO2,防止污染空气.
(2)某无土栽培营养液的配方中可能含有氯化钾、硫酸铵、碳酸氢铵中的一种或几种物质,为确定配方的成分,化学兴趣小组的同学开展了以下探究活动:
(1)【实验探究一】取少量固体样品在研体中与熟石灰混合研磨,有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变蓝色,写出可能发生该反应的一个化学方程式NH4HCO3+Ca(OH)2=CaCO3+NH3↑+2H2O或(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O.
(2)【实验探究二】另取少量固体样品溶于水得到溶液A,按下图所示进行实验,现象如图所述(设发生的反应都恰好完全进行).请你回答下列问题:

①白色沉淀E是硫酸钡.
②小明认为由实验探究二可以确定该化肥中一定含有氯化钾和硫酸铵,一定没有碳酸氢铵.小强认为这个结论不正确,他的理由步骤Ⅰ中加入的稀盐酸引入了氯离子,影响了氯化钾的检验.为了使小明的结论正确,小强对上述实验进行了改动,他的做法是将步骤Ⅰ中的稀盐酸换为稀硝酸.
分析 (1)①根据实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热进行分析;
根据催化剂的定义进行分析;
根据过氧化氢在二氧化锰的催化作用下加热生成水和氧气进行分析;
②根据被测定气体的性质不溶于水且不与水反应进行分析;
③根据浓硫酸有吸水性,二氧化硫有毒进行分析.
(1)根据氨气溶于水显碱性能使湿润的红色石蕊试纸变蓝色以及铵态氮肥遇碱放出氨气进行解答;
(2)根据硝酸钡和硫酸铵反应生成硫酸钡沉淀和硝酸铵以及步骤Ⅰ中加入的稀盐酸引入了氯离子,影响了氯化钾的检验进行解答.
解答 解:(1)①实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,所以选择的发生装置是:A,二氧化锰在氯酸钾制取氧气的过程中是催化剂,可以加快反应的速率,所以实验过程中发现产生氧气的速率很慢,可能的原因是:未加二氧化锰,若用B、C装置制取氧气,反应物应该是液体,B中发生的反应是过氧化氢在二氧化锰的催化作用下反应生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②被测定气体的性质不溶于水且不与水反应,所以气体应从b进入F中;
③浓硫酸有吸水性,在洗气时,应该长进短出,所以装置的导管按气流方向连接的顺序是:d→c→a→b→e,二氧化硫有毒,所以装置的H的作用是:吸收多余的SO2,防止污染空气.
(2)
(1)氨气溶于水显碱性能使湿润的红色石蕊试纸变蓝色,铵态氮肥遇碱放出氨气,可能发生该反应的化学方程式是NH4HCO3+Ca(OH)2=CaCO3+NH3↑+2H2O或(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;故填:蓝;NH4HCO3+Ca(OH)2=CaCO3+NH3↑+2H2O或(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;
(2)①硝酸钡和硫酸铵反应生成硫酸钡沉淀和硝酸铵,白色沉淀E是硫酸钡;故填:硫酸钡;
②步骤Ⅰ中加入的稀盐酸引入了氯离子,影响了氯化钾的检验,为了使小明的结论正确,小强对上述实验进行了改动,他的做法是将步骤Ⅰ中的稀盐酸换为稀硝酸.故填:步骤Ⅰ中加入的稀盐酸引入了氯离子,影响了氯化钾的检验;将步骤Ⅰ中的稀盐酸换为稀硝酸.
故答案为:
(1)①A,未加二氧化锰,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②b;
③d→c→a→b,吸收多余的SO2,防止污染空气.
(2)
(1)【实验探究一】蓝;NH4HCO3+Ca(OH)2=CaCO3+NH3↑+2H2O或(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;
(2)【实验探究二】①硫酸钡
②步骤Ⅰ中加入的稀盐酸引入了氯离子,影响了氯化钾的检验;将步骤Ⅰ中的稀盐酸换为稀硝酸.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强,气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

| A. |  | B. |  | C. |  | D. |  |
| A. |  点燃酒精灯 | B. |  打开瓶盖吸少量液体 | ||
| C. |  给液体加热 | D. |  滴加液体 |
| A[性质与用途] ①CO具有还原性--用于冶炼金属 ②石墨具有导电性--作电极 | B[物质的分类] 由多种物质组成--混合物 含有氧元素的化合物--氧化物 |
| C[安全知识] ①碰倒酒精灯致洒出的酒精在桌上燃烧--立即用湿布盖灭 ②皮肤上不慎沾上氢氧化钠溶液--用大量的水冲洗,再涂上硼酸溶液 | D[生活经验] ①区分白酒和白醋--闻气味 ②刚装修好的房间不易立即入住--会挥发出甲醛污染空气,应选择不含甲醛的绿色环保产品 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氮气可以作保护气,说明氮气不与任何物质反应 | |
| B. | 水和过氧化氢组成元素相同,所以化学性质也相同 | |
| C. | 蔗糖的饱和溶液不能再溶解蔗糖,也一定不能再溶解其他物质 | |
| D. | 某物质燃烧生成CO2和H2O,则该物质的组成中一定含有碳、氢元素 |
| A. | 冰雪消融 | B. | 酒精挥发 | C. | 食物腐烂 | D. | 活性炭除臭 |
【提出问题】金属与硫酸反应快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的浓度有关;b.可能与反应时的温度有关.
【设计并实验】小明用不同质量分数的硫酸和相同形状的锌进行如表实验.
| 实验编号 | 硫酸的质量分数 (均取20mL) | 温度/℃ | 收集40mL气体所需时间/秒 |
| ① | 5% | 30 | 48 |
| ② | 10% | 20 | 41 |
| ③ | 5% | 20 | 69 |
| ④ | 10% | 30 | 32 |
(1)写出锌与硫酸反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.
(2)通过实验①③相比,说明其它条件相同,温度越高,反应速率越快;通过实验②③或①④(写编号)说明反应物浓度对反应快慢有影响.
(3)如果硫酸质量分数为5%,温度为25℃,则收集40mL气体所需的时间范围为48s~69s.
【反思】
(1)小明在做以上四组反应时,发现一开始反应速率都很慢,原因是实验前没有除去锌表面的氧化膜.
(2)浓度相同,颗粒大小可能影响化学反应的速率,请设计实验方案进行验证在30℃时,向两支试管中分别加入5g锌粉、锌粒,再分别取20mL10%的稀盐酸,测定收集40mL气体所需的时间.
(3)影响金属与酸反应快慢的因素还有很多,请你再设计实验探究一种因素的影响.取两份相同浓度、相同体积的稀硫酸,在相同温度下,加入相同的片状的锌和铝,比较收集相同体积的氢气所需的时间.
| A. | 电路着火,用水浇 | |
| B. | 室内着火,打开所有的门窗 | |
| C. | 图书档案失火时选用二氧化碳灭火器灭火 | |
| D. | 发现煤气泄漏时,立即打开排气扇 |