题目内容
1.从化学方程式2KClO3 $\frac{\underline{\;MnO_{2}\;}}{△}$ 2KCl+3O2↑中获取的信息错误的是( )| A. | 反应生成了气体 | |
| B. | 反应物是KClO3和MnO2,生成物是KCl和O2 | |
| C. | 反应物与生成物的粒子个数比为2:2:3 | |
| D. | 245g KClO3完全反应生成149g KCl和96g O2 |
分析 只有熟悉反应物、生成物和反应条件,依据质量守恒定律的两个原则、书写化学方程式的书写的方法和步骤,就可以写出正确的化学方程式.
解答 解:根据质量守恒定律,反应前后原子个数相等,
A、反应生成了气体,正确;
B、反应物是KClO3,生成物是KCl和O2,错误;
C、反应物与生成物的粒子个数比为2:2:3,正确;
D、245g KClO3完全反应生成149g KCl和96gO2,正确;
故选B
点评 化学方程式经常出现的错误有:化学式写错、没配平,漏掉反应条件和生成物的状态符号.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
16.某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.
【查阅资料】
天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
根据上述物质的溶解性,小组同学确定水垢的主要成分中一定含有的两种物质是,可能含有Ca(OH)2和MgCO3.
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)2
【实验方案2】确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究.其主要实验步骤如下:
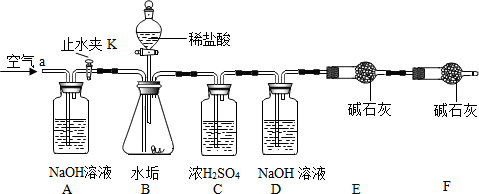
按如图组装后,将9.8g水垢试样放入锥形瓶中,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后精确称量D、E装置总质量为600.0g关闭止水夹K,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处再次缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(注意:碱石灰主要成分为CaO和NaOH的混合物).
【实验讨论】
(1)加入药品前应;待锥形瓶中不再产生气泡时,打开止水夹K,缓缓鼓入空气的目的是.
(2)C装置的作用是:干燥生成的气体.
(3)装置 B中生成CO2的质量为4.4g.通过计算说明该水垢中(填序号)含MgCO3.
A.一定B.一定不C.可能D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出计算过程,结果保留1位小数).
【反思】缺少F装置会使所测水垢样品中氢氧化镁的质量分数偏小(填写“偏大”或“偏小”或“不变”).
【查阅资料】
天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
| 阴离子 阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)2
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 无白色沉淀 | 水垢中无Ca(OH)2 |
利用下列实验装置,完成实验2探究.其主要实验步骤如下:

按如图组装后,将9.8g水垢试样放入锥形瓶中,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后精确称量D、E装置总质量为600.0g关闭止水夹K,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处再次缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(注意:碱石灰主要成分为CaO和NaOH的混合物).
【实验讨论】
(1)加入药品前应;待锥形瓶中不再产生气泡时,打开止水夹K,缓缓鼓入空气的目的是.
(2)C装置的作用是:干燥生成的气体.
(3)装置 B中生成CO2的质量为4.4g.通过计算说明该水垢中(填序号)含MgCO3.
A.一定B.一定不C.可能D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出计算过程,结果保留1位小数).
【反思】缺少F装置会使所测水垢样品中氢氧化镁的质量分数偏小(填写“偏大”或“偏小”或“不变”).
6.下列操作正确的是( )
| A. | 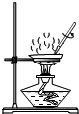 蒸发溶剂 | B. |  稀释浓硫酸 | ||
| C. | 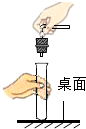 在桌面上塞上橡皮塞 | D. | 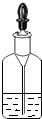 滴瓶上的滴管清洗后放回 |
13.运用2008年诺贝尔化学奖的研究成果,可依据生物发光现象检测超微量钙的存在.这里的“钙”是指( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 单质 |
10. 在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按如图所示流程进行实验,请你参与讨论并回答相关问题
在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按如图所示流程进行实验,请你参与讨论并回答相关问题
(1)操作Ⅰ中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是使液体受热均匀,防止液滴飞溅.
【问题与发现】该小组同学所得到固体C一定是纯净的NaOH吗?
【猜想与假设】根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH
乙:NaOH和Na2CO3的混合物
丙:NaOH和Ca(OH)2的混合物
【探究与实验】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.实验操作、现象和结论如表,请参与他们的探究并填补上所缺内容.
【反思与评价】同学们认真研究实验流程,讨论后一致认为乙、丙两位同学的方案、现象和推理均为正确,甲同学设计的方案不严密(填写“严密”或“不严密”),理由是纯碱溶液和氢氧化钙溶液均显碱性,无论哪种物质过量,均能使酚酞试液变红.
 在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按如图所示流程进行实验,请你参与讨论并回答相关问题
在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按如图所示流程进行实验,请你参与讨论并回答相关问题(1)操作Ⅰ中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是使液体受热均匀,防止液滴飞溅.
【问题与发现】该小组同学所得到固体C一定是纯净的NaOH吗?
【猜想与假设】根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH
乙:NaOH和Na2CO3的混合物
丙:NaOH和Ca(OH)2的混合物
【探究与实验】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.实验操作、现象和结论如表,请参与他们的探究并填补上所缺内容.
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞溶液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量稀盐酸 | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液 | 出现白色沉淀 | 猜想成立 |