题目内容
18.某工厂排放的废水中含有少量硫酸,需经处理呈中性后排放.小明取废液样品30g于烧杯中,向其中逐渐滴加2%的NaOH溶液,并不断搅拌,恰好完全反应时,消耗掉NaOH溶液20g.分析并计算:
(1)用pH试纸或者pH计可以测定溶液的酸碱度.
(2)计算恰好完全反应时,所得溶液中溶质的质量分数(结果精确到0.01%).
分析 (1)测定酸碱度用pH试纸或者pH计,检验酸碱性用酸碱指示剂;
(2)根据消耗的氢氧化钠的质量和对应的化学方程式求算生成的硫酸钠的质量,进而求算其质量分数.
解答 解:测定溶液的酸碱度用pH试纸或者pH计.
所用的氢氧化钠溶液中氢氧化钠的质量为20g×2%=0.4g
设生成的硫酸钠的质量为x
H2SO4+2NaOH=Na2SO4+2H2O
80 142
0.4g x
$\frac{80}{142}$=$\frac{0.4g}{x}$
x=0.71g
恰好完全反应时,所得溶液中溶质的质量分数为$\frac{0.71g}{30g+20g}$×100%=1.42%
答:(1)用 pH试纸或者pH计可以测定溶液的酸碱度.
(2)恰好完全反应时,所得溶液中溶质的质量分数为1.42%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
6.下列家庭实验中不涉及化学变化的是( )
| A. | 用少量食醋除去水壶中的水垢 | B. | 家庭自酿葡萄酒 | ||
| C. | 用木炭除去冰箱中的异味 | D. | 燃烧蜡烛制取少量炭黑 |
9.归纳与比较”是化学学习的主要方法.下列关于CO2与CO的不同点比较错误的是( )
| A. | 组成:组成元素相同,碳元素的化合价不同 | |
| B. | 性质:CO2能溶于水,与水反应生成碳酸; CO难溶于水,但能燃烧 | |
| C. | 用途:CO2可用于光合作用、灭火等; CO可作气体燃料,还可用于人工降雨 | |
| D. | 危害:CO2会造成“温室效应”; CO易与血液中的血红蛋白结合引起中毒 |
6.亮亮做家务时接触到下列用品,请分析回答问题.
(1)清理垃圾时,亮亮发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁粉生锈的原因是Fe与潮湿的空气接触.
(2)亮亮刷洗马桶时,不小心将洁厕灵倒在大理石地砖上,可能看到的现象是产生气泡.
(3)亮亮清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
| 用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(2)亮亮刷洗马桶时,不小心将洁厕灵倒在大理石地砖上,可能看到的现象是产生气泡.
(3)亮亮清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
3.有一包白色粉末,可能含有氯化钡、氢氧化钠、氯化铵、碳酸钠、硫酸铜、硫酸钠中的一种或几种.为确定其组成,进行下列实验:
①将该白色粉末溶于足量的水中,产生白色沉淀和无色溶液,过滤;
②将①中滤液分成二份,向一份中滴加酚酞试液,溶液变红;向另一份中滴加硝酸银溶液,溶液变浑浊;
③将①中滤渣投入足量的稀盐酸中,白色固体部分溶解.
则下列说法不正确的是( )
①将该白色粉末溶于足量的水中,产生白色沉淀和无色溶液,过滤;
②将①中滤液分成二份,向一份中滴加酚酞试液,溶液变红;向另一份中滴加硝酸银溶液,溶液变浑浊;
③将①中滤渣投入足量的稀盐酸中,白色固体部分溶解.
则下列说法不正确的是( )
| A. | 白色粉末中肯定有氯化钡、氢氧化钠、硫酸钠和碳酸钠 | |
| B. | ①中的滤液里可能含有碳酸钠 | |
| C. | 白色粉末中肯定有氯化钡、硫酸钠和碳酸钠,可能有氢氧化钠 | |
| D. | 若在①中滤液中滴加稀盐酸产生气泡,则白色粉末中肯定有碳酸钠和氯化钡,且二者的质量比一定为$\frac{m(N{a}_{2}C{O}_{3})}{m(BaC{l}_{2})}$>$\frac{106}{208}$ |
7.如图是X原子的结构示意图和X元素在元素周期表中的信息.下列关于X的说法正确的是( )

| A. | X原子失电子后形成的离子是X3- | B. | 相对原子质量是26.98 g | ||
| C. | 原子核内中子数为13 | D. | y=3 |
8.下列物品所使用的主要材料为有机合成材料的是( )
| A. | 橡胶轮胎 | B. | 纯棉帽子 | C. | 黄金首饰 | D. | 陶瓷花瓶 |

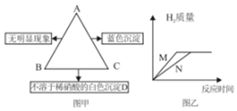 有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:
有A、B、C三种物质,已知A是一种氯化物(RCl2),B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答: