题目内容
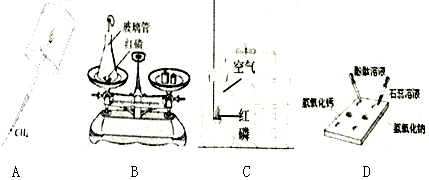
5. 在今年化学实验操作考试“探究纯碱的性质”中,同学们做了如图所示的四组实验,并将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中.考试结束后,某兴趣小组发现大烧杯底部有沉淀,上层溶液呈红色.为了探究上层溶液的成分,进行了以下实验.
在今年化学实验操作考试“探究纯碱的性质”中,同学们做了如图所示的四组实验,并将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中.考试结束后,某兴趣小组发现大烧杯底部有沉淀,上层溶液呈红色.为了探究上层溶液的成分,进行了以下实验.【提出问题】大烧杯中的上层溶液中除了含有水和酚酞外,还含有哪些离子?(假设难溶物质、水和酚酞均不会解离出离子)
【猜想假设】小明认为上层溶液中一定含有Na+、CO32-、H+、Cl-、Ba2+、Ca2+、OH-七种离子,你认为上层溶液中含有的离子最多可能有几种,它们分别是Na+、Cl-、Ba2+、Ca2+、OH-(填离子符号).
【分析讨论】(1)小红认为上层溶液中一定不含有H+,因为上层溶液呈红色.请你分析上层溶液中不含有H+的另外一个理由氢离子和氢氧根离子不能共存.
(2)小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一定不含有CO32-.小红认为他的结论不正确,原因是酸碱优先反应,如果所加盐酸过少,被碱全部消耗,没与CO32-反应.
【设计实验】为进一步确定上层溶液中是否含有CO32-,请你和小红一起参与下列探究:
| 实验操作 | 实验现象 | 实验结论 |
| 取大烧杯中上层溶液少许于一支试管中,滴加过量的BaCl2溶液,静置 | ① 有白色沉淀生成 ②试管中 的上层溶液仍是红色 | ①大烧杯中上层溶液中一定含有CO32- ②同时还能得出大烧杯中的上层溶液中一定含有离子是 OH-(填离子符号) |
分析 【猜想假设】根据已有的离子的性质以及离子间结合时的实验现象进行分析解答即可.
【分析讨论】(1)根据氢离子和氢氧根离子不能共存解答;
(2)根据酸碱优先反应,如果所加盐酸过少,被碱全部消耗,没与CO32-反应,解答;
解答 解:
【猜想假设】将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中,上层溶液呈红色,说明溶液呈碱性,故一定含有氢氧根离子,不含有氢离子;大烧杯底部有沉淀,Ba2+、Ca2+与CO32-反应能产生碳酸钡、碳酸钙沉淀,上层溶液中Ba2+、Ca2+与CO32-不能共存,故上层溶液中含有的离子最多可能有5中,它们分别是Na+、Cl-、Ba2+、Ca2+、OH-;
【分析讨论】(1)小红认为上层溶液中一定不含有H+,因为上层溶液呈红色.上层溶液中不含有H+的另外一个理由氢离子和氢氧根离子不能共存;
(2)小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一定不含有CO32-.小红认为他的结论不正确,原因是:酸碱优先反应,如果所加盐酸过少,被碱全部消耗,没与CO32-反应;
【设计实验】与氯化钡反应生成白色沉淀的是碳酸根离子和硫酸根离子,
取大烧杯中上层溶液少许于一支试管中,滴加过量的BaCl2溶液,静置,①有白色沉淀生成,说明大烧杯中上层溶液中一定含有CO32-;
②试管中的上层溶液仍是红色,说明溶液呈碱性,同时还能得出大烧杯中的上层溶液中一定含有离子是OH-.
【实验结论】大烧杯中的上层溶液中一定含有的离子是CO32-、OH-.
答案:
【猜想假设】Na+、Cl-、Ba2+、Ca2+、OH-;
【分析讨论】
(1)氢离子和氢氧根离子不能共存;
(2)酸碱优先反应,如果所加盐酸过少,被碱全部消耗,没与CO32-反应;
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取大烧杯中上层溶液少许于一支试管中,滴加过量的BaCl2溶液,静置 | ① 有白色沉淀生成 ②试管中 的上层溶液仍是红色 | ①大烧杯中上层溶液中一定含有CO32- ②同时还能得出大烧杯中的上层溶液中一定含有离子是 OH-(填离子符号) |
点评 本题考查的是常见的离子的检验,完成此题,可以依据已有的离子的性质以及检验的方法进行.本题是一个综合性很强的实验题,难度较大.试题涉及到了试验设计、常见离子组的鉴别.学生对方程式的书写应熟练掌握.

 阅读快车系列答案
阅读快车系列答案| A. | 氢氧化钠可用于治疗胃酸过多症 | |
| B. | 工业上一般用焦炭、石灰石和铁矿石炼铁 | |
| C. | 金刚石的硬度大可用于切割玻璃 | |
| D. | 氮气的化学性质不活泼,常用作保护气 |
| A. | 纯碱、Na2CO3 | B. | 烧碱、NaOH | C. | 生石灰、CaO | D. | 石灰石、Ca(OH)2 |
| A. | 红磷在空气中燃烧,产生大量的白雾 | |
| B. | 铁丝浸入稀盐酸,形成黄色溶液 | |
| C. | 持续加热碳酸氢钠,最终没有固体残留 | |
| D. | 向氢氧化钠溶液中加入硫酸铜溶液有蓝色沉淀生成 |
| A. | 回收输液器再利用,做成食品塑料袋 | |
| B. | 推广无纸化办公,使用再生纸且双面打印 | |
| C. | 大力发展新资源,禁止使用化石燃料 | |
| D. | 把废水利用高压泵打入地下,减少对河流污水的排放 |
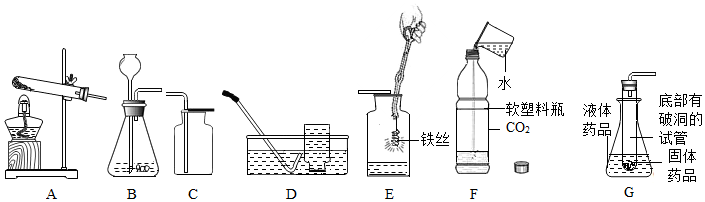
 (1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.
(1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.