题目内容
6.下列四个图象反映了对应实验过程中相关量的变化,其中不正确的是( )| A. |  向一定量因长期存放而变质的NaOH溶液中滴加澄清石灰水 向一定量因长期存放而变质的NaOH溶液中滴加澄清石灰水 | |
| B. |  O2的溶解度受温度影响的变化曲线 O2的溶解度受温度影响的变化曲线 | |
| C. | 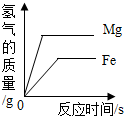 等质量的Mg粉和Fe粉与足量同浓度的稀硫酸反应 等质量的Mg粉和Fe粉与足量同浓度的稀硫酸反应 | |
| D. | 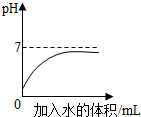 硫酸溶液稀释过程中pH的变化曲线 硫酸溶液稀释过程中pH的变化曲线 |
分析 A、依据部分变质的氢氧化钠中含有碳酸钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀分析解答;
B、依据气体的溶解度随温度的升高而降低的原理分析解答;
C、依据两者的金属活动性顺序的应用分析解答;
D、依据硫酸稀释后的酸性变化情况分析解答.
解答 解:A、由于部分变质的氢氧化钠中含有碳酸钠,而放入石灰水后要与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故开始沉淀增加,碳酸钠反应完全后沉淀质量不会变化;正确;
B、由于气体的溶解度随温度的升高而降低,所以该图象应该是一条下降的曲线;错误;
C、镁的金属活动性比铁强,故与稀盐酸反应时镁的反应速度要快一些(图象更陡一些),由于金属与酸反应生成氢气的质量=金属的质量×$\frac{金属的化合价}{金属的相对原子质量}$,所以同质量的镁要比铁生成的氢气要多,故最终镁的曲线应该在铁的上面;正确;
D、由于硫酸稀释时酸性会不断减弱,故其pH会不断增大,但不管怎样稀释溶液也不会呈中性,即溶液的pH只能永远的接近7但不会达到7;正确;
故选B.
点评 根据曲线的纵横坐标轴的说明,判断曲线所表示的变化关系,此是正确答题的根本.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
10.下列对有关燃烧及灭火事例的解释错误的是( )
| A. | 用扇子扇煤炉,炉火越扇越旺-给煤燃烧提供充足的氧气 | |
| B. | 用嘴吹燃着的蜡烛,蜡烛熄灭-降低了可燃物的着火点 | |
| C. | 炒菜时油锅着火,用锅盖盖灭-隔绝了空气 | |
| D. | 酒精洒到实验台上着火,用湿布覆盖-隔绝空气又降低了温度 |
1.通过一年的化学学习,同学们建立的下列观点中正确的是( )
| A. | 熟石灰可用来改良酸性土壤,因为熟石灰呈碱性 | |
| B. | 洗涤剂常用来洗涤油污,因为洗涤剂能把油污溶解 | |
| C. | “银粉漆”(铝粉)可涂在铁栏杆上防锈,因为铝的化学性质稳定 | |
| D. | 一氧化碳用于冶炼金属,因为一氧化碳具有可燃性 |
11.为保证实验安全,取得预期实验效果,我们应正确进行实验操作丙遵循化学实验的安全规则.下列A~G七项实验操作中有三项是不正确的,请写出不正确操作的序号( )
| A. | 取用液体药品时,要把瓶塞倒放在桌面上,标签朝向手心,放回原处时标签向外. | |
| B. | 给试管里的液体加热时,不要把拇指按在试管夹短柄上,试管口不能对着自己和他人,试管内液体不超过试管容积的三分之一 | |
| C. | 为了便于观察,可用于接触药品,可以将鼻孔凑到药品的附近闻气味,但严禁品尝药品. | |
| D. | pH值试纸的用法,用镊子夹持pH试纸条将其一端浸入待测液,看到起颜色不发生变化时取出与标准比色卡比较,得出其pH值. | |
| E. | 配制稀硫酸时,将浓硫酸沿烧杯壁慢慢加入水中,并不断搅拌 | |
| F. | 切忌向燃着的酒精灯内添加酒精,可用燃着的酒精灯点燃另一个酒精灯 | |
| G. | 取用一定质量的NaOH固体时,应将其放在玻璃器皿中进行称量 |
16. 食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.
食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.
【提出问题】该脱氧剂中的黑色是什么?
【提出猜想】黑色粉末可能含炭粉、铁粉、氧化铜中的一种或几种.
【进行实验】
【得出结论】由实验①②可知,脱氧剂中黑色粉末肯定含铁粉、碳粉肯定不含铜,写出实验①过程中发生的一个相应的化学方程式Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
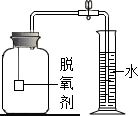
【拓展延伸】小明认为铁生锈时会消耗氧气,因此可用此脱氧剂(实验室可滴几滴水)测定空气中氧气的含量,装置如图所示.集气瓶的实际容积是150mL,量筒内盛100mL的水.当量筒 内水面不再变化,且温度回复至室温时,读出水面在73mL刻度处.由上述实验数据可以算出,空气中氧气的体积分数是18%.本实验的测量结果与理论值不一致,原因可能是脱氧剂不足等.
 食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.
食品包装袋中常用脱氧剂.某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末.【提出问题】该脱氧剂中的黑色是什么?
【提出猜想】黑色粉末可能含炭粉、铁粉、氧化铜中的一种或几种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取脱氧剂黑色粉末加入足量稀硫酸 | 粉末几乎全部溶解,只有少量黑色粉末未溶解,有气泡产生,溶液为浅绿色色 |
| ② | 实验①的残渣灼烧,将内壁有 澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
【拓展延伸】小明认为铁生锈时会消耗氧气,因此可用此脱氧剂(实验室可滴几滴水)测定空气中氧气的含量,装置如图所示.集气瓶的实际容积是150mL,量筒内盛100mL的水.当量筒 内水面不再变化,且温度回复至室温时,读出水面在73mL刻度处.由上述实验数据可以算出,空气中氧气的体积分数是18%.本实验的测量结果与理论值不一致,原因可能是脱氧剂不足等.
 运用所学的科学知识回答:
运用所学的科学知识回答:
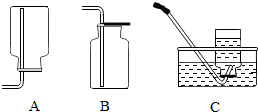 小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:
小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究: