题目内容
19.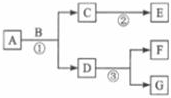 A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素.它们在一定条件下转化关系如图所示,其中部分反应物或生成物已略去. 请针对以下两种情况回答问题.
A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素.它们在一定条件下转化关系如图所示,其中部分反应物或生成物已略去. 请针对以下两种情况回答问题.若A中两种元素的质量比为7:3,F是一种红色金属,则F的化学式为Cu;写出反应①、③的化学方程式:①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;③Fe+CuSO4═FeSO4+Cu.
分析 根据题目给出的流程图和信息:已知Fe+CuSO4═Cu+FeSO4,F是一种红色金属,则可知F是铜,D是铁,G是FeSO4;因为A与G含有相同的金属元素,A中两种元素的质量比为7:3,因为三氧化二铁中铁和氧两种元素的质量比为:112:48=7:3,故可知A物质是三氧化二铁;氧化铁和一氧化碳在高温的条件下生成铁和二氧化碳,配平即可.故可以根据物质的性质及其物质相互作用的实验现象等方面进行综合分析、判断,从而得出正确的结论.
解答 解:根据题目给出的流程图和信息:已知Fe+CuSO4═Cu+FeSO4,F是一种红色金属,则可知F是铜,D是铁,G是FeSO4;因为A与G含有相同的金属元素,A中两种元素的质量比为7:3,因为三氧化二铁中铁和氧两种元素的质量比为:112:48=7:3,故可知A物质是三氧化二铁;反应①氧化铁和一氧化碳在高温的条件下生成铁和二氧化碳,配平即可,故其化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;或三氧化二铁和氢气反应生成铁和水,配平即可,故其化学方程式为Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O.反应③铁和硫酸铜反应生成硫酸亚铁和红色的铜,故其化学方程式为Fe+CuSO4═FeSO4+Cu.
故答案为:
Cu;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2或Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O;Fe+CuSO4═FeSO4+Cu
点评 本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.

 初中学业考试导与练系列答案
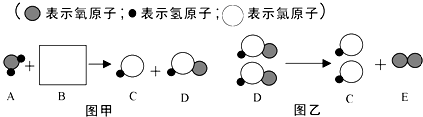
初中学业考试导与练系列答案| A. | 表示过氧化氢这种物质 | |
| B. | 表示一个过氧化氢分子由一个氧气分子和一个氢气分子组成 | |
| C. | 表示过氧化氢由氢元素和氧元素组成 | |
| D. | 表示1个过氧化氢分子 |
| A. | 生铁和钢的性能不同--含碳量不同 | |
| B. | 硫和磷的元素种类不同--质子数不同 | |
| C. | 一氧化碳和二氧化碳的化学性质不同--氧原子个数不同 | |
| D. | 硫在空气和氧气中燃烧的火焰颜色不同--氧气浓度不同 |