题目内容
7.对于化学式H2O2的意义描述错误的是( )| A. | 表示过氧化氢这种物质 | |
| B. | 表示一个过氧化氢分子由一个氧气分子和一个氢气分子组成 | |
| C. | 表示过氧化氢由氢元素和氧元素组成 | |
| D. | 表示1个过氧化氢分子 |
分析 根据双氧水的化学式为H2O2,可知表示过氧化氢这种物质,表示1个过氧化氢分子,表示过氧化氢是由氢、氧两种元素组成,表示1个过氧化氢分子是由2个氢原子和2个氧原子构成来解答.
解答 解:A.H2O2表示过氧化氢这种物质,故A说法正确;
B.H2O2表示1个过氧化氢分子,1个过氧化氢分子是由2个氢原子和2个氧原子构成;故B说法错误;
C.H2O2表示过氧化氢是由氢、氧两种元素组成,故C说法正确;
D.H2O2表示1个过氧化氢分子,故D说法正确;
故选B.
点评 本题考查化学式的意义,明确化学式的组成和构成是解答的关键,并注意组成和构成在描述上的差别,不可混淆.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
8.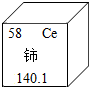 稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
 稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )| A. | 铈的原子序数为58 | B. | 铈的相对原子质量为140.1g | ||
| C. | 铈属于金属元素 | D. | 铈的质子数为58 |
16.下列各组日常生活中发生的变化,都属于化学变化的是( )
| A. | 酒精燃烧 蜡烛熔化 | B. | 干冰升华 轮胎爆炸 | ||
| C. | 剩饭变馊 高粱酿酒 | D. | 灯泡发光 铁锅生锈 |
17.某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律:

实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)
过一会再称量.数据见表:
(1)在实验Ⅰ中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释反应后生成的氧化镁的质量等于反应的镁的质量和反应的氧气质量的和.
(2)实验Ⅱ中发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
(3)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因反应前后,原子种类不变,原子总个数不变,原子的质量不变.
(4)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验Ⅱ中,不当之处是反应装置是敞开的;应该改进为:把锌粒和稀盐酸放在密闭容器中.

实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)
过一会再称量.数据见表:
| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)实验Ⅱ中发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
(3)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因反应前后,原子种类不变,原子总个数不变,原子的质量不变.
(4)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验Ⅱ中,不当之处是反应装置是敞开的;应该改进为:把锌粒和稀盐酸放在密闭容器中.
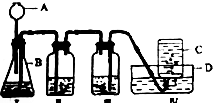 下面是实验室制取二氧化碳并验证其性质的实验装置图(Ⅲ中装澄清石灰水,Ⅱ中装置紫色石蕊试液).回答下列问题.
下面是实验室制取二氧化碳并验证其性质的实验装置图(Ⅲ中装澄清石灰水,Ⅱ中装置紫色石蕊试液).回答下列问题.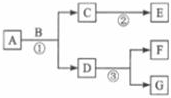 A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素.它们在一定条件下转化关系如图所示,其中部分反应物或生成物已略去. 请针对以下两种情况回答问题.
A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素.它们在一定条件下转化关系如图所示,其中部分反应物或生成物已略去. 请针对以下两种情况回答问题.