题目内容
煤等化石燃料燃烧时产生的SO2会对大气造成污染.如果某火力发电厂每秒燃烧10kg 煤,煤中硫元素的质量分数为1%.假设煤中的硫全部转化为SO2,试计算该发电厂每天产生的SO2的物质的量是多少?
考点:化合物中某元素的质量计算,混合物中某元素的质量计算
专题:化学式的计算
分析:根据煤中硫元素的质量分数为1%,计算10kg煤中硫元素的质量,由n=
计算硫原子的物质的量,根据硫元素守恒可知n(SO2)=n(S).
| m |
| M |
解答:解:n(SO2)=n(S)=1000g/kg×10kg×1%×24×3600/32g/mol
=270000mol
答:该发电厂每天产生的SO2的物质的量为270000mol.
=270000mol
答:该发电厂每天产生的SO2的物质的量为270000mol.
点评:本题考查化学有关的计算,注意利用硫元素守恒进行计算,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于原子的叙述正确的是( )
| A、原子一定比分子小 |
| B、一切物质都是由原子直接构成的 |
| C、同种原子内的质子数相同 |
| D、含有相同中子数的原子,一定是同一种原子 |
分别将下列各组物质同时加到足量的水中,能大量共存,且得到无色透明溶液的是( )
| A、H2SO4、NaNO3、Na2SO4 |
| B、NaNO3、Ba(OH)2、HNO3 |
| C、H2SO4、NaNO3、FeSO4 |
| D、CaCl2、Na2SO4、BaCl2 |
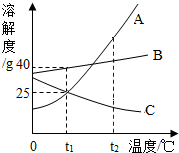 如图为A、B、C三种物质的溶解度曲线.根据曲线回答下列问题.
如图为A、B、C三种物质的溶解度曲线.根据曲线回答下列问题. 在校园科技节上,小天同学表演了一个魔术,他将一个鸡蛋(注:鸡蛋壳的主要成分是碳酸钙)放入烧杯中,向该烧杯中倒入稀盐酸,不久他看到烧杯中出现
在校园科技节上,小天同学表演了一个魔术,他将一个鸡蛋(注:鸡蛋壳的主要成分是碳酸钙)放入烧杯中,向该烧杯中倒入稀盐酸,不久他看到烧杯中出现 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组的同学称取该样品20g放入烧杯中,向其中逐滴加入稀硫酸,反应过程中生成的气体与所用稀硫酸溶液的质量关系如右图所示,请计算:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组的同学称取该样品20g放入烧杯中,向其中逐滴加入稀硫酸,反应过程中生成的气体与所用稀硫酸溶液的质量关系如右图所示,请计算: