题目内容
碳酸氢钠是一种用途广泛的盐,某实验小组的同学设计了以下实验,以探究碳酸氢钠的性质.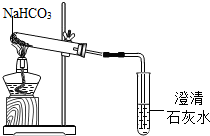
【探究实验1】碳酸氢钠的物理性质:用 (写仪器名称)取少量固体放入试管中,加入适量水充分振荡.现象:固体为白色粉末,加水后固体 .结论:碳酸氢钠能溶于水.
【探究实验2】碳酸氢钠溶液的酸碱性:在上述溶液中滴入几滴酚酞试液,振荡.现象:溶液变成红色.由此得出的结论是 .
【探究实验3】能否与酸反应:取少量固体放入试管中,加入稀盐酸,现象为 .结论:碳酸氢钠能与酸反应.
【探究实验4】碳酸氢钠的热稳定性:用如图所示装置进行实验.大试管口略向下倾斜的原因是
;现象:充分加热后,大试管壁上有水珠出现,管底有白色固体残留,小试管中澄清石灰石变浑浊;结论:碳酸氢钠受热能分解,分解的反应方程式是 ;
验证:请你帮他们设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH,实验方法和现象是 .
【拓展应用】试说出碳酸氢钠在日常生活中的一种用途 .

【探究实验1】碳酸氢钠的物理性质:用
【探究实验2】碳酸氢钠溶液的酸碱性:在上述溶液中滴入几滴酚酞试液,振荡.现象:溶液变成红色.由此得出的结论是
【探究实验3】能否与酸反应:取少量固体放入试管中,加入稀盐酸,现象为
【探究实验4】碳酸氢钠的热稳定性:用如图所示装置进行实验.大试管口略向下倾斜的原因是
验证:请你帮他们设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH,实验方法和现象是
【拓展应用】试说出碳酸氢钠在日常生活中的一种用途
考点:盐的化学性质,常用盐的用途,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:[探究实验1]取用粉末状药品用药匙,并据结论分析现象;
[探究实验2]碱性溶液能使酚酞试液变红;
[探究实验3]碳酸盐和酸反应生成二氧化碳;
[探究实验4]加热碳酸氢钠生成水,所以试管口要低于试管底部,防止水倒流引起试管炸裂;并据现象分析碳酸氢钠分解的生成物,书写方程式;
验证:鉴别碳酸钠和氢氧化钠可根据二者化学性质的不同,滴加酸观察是否有气泡产生、或滴加澄清的石灰水或可溶性钙盐的溶液,根据是否生成沉淀加以区别;
[拓展应用]根据碳酸氢钠的性质推测其用途.
[探究实验2]碱性溶液能使酚酞试液变红;
[探究实验3]碳酸盐和酸反应生成二氧化碳;
[探究实验4]加热碳酸氢钠生成水,所以试管口要低于试管底部,防止水倒流引起试管炸裂;并据现象分析碳酸氢钠分解的生成物,书写方程式;
验证:鉴别碳酸钠和氢氧化钠可根据二者化学性质的不同,滴加酸观察是否有气泡产生、或滴加澄清的石灰水或可溶性钙盐的溶液,根据是否生成沉淀加以区别;
[拓展应用]根据碳酸氢钠的性质推测其用途.
解答:解:[探究实验1]
由题意可知:碳酸氢钠是白色粉末,取用粉末状药品用药匙,根据实验结论:碳酸氢钠能溶于水,所以加水后固体会消失、溶解;
【探究实验2】因为碱性溶液能使酚酞变红,所以滴入几滴酚酞试液,振荡.溶液变成红色,说明碳酸氢钠溶液呈碱性;
[探究实验3]
碳酸氢钠和盐酸反应生成二氧化碳气体,所以会看到溶液中能产生气泡;
[探究实验4]
加热碳酸氢钠生成水,所以试管口要低于试管底部,防止水倒流引起试管炸裂;碳酸氢钠充分加热后,大试管壁上有水珠出现,说明生成水,管底有白色固体残留,小试管中澄清石灰石变浑浊,说明生成二氧化碳,据反应前后元素种类不变,可知生成的白色固体是碳酸钠,方程式是:2NaHCO3
Na2CO3+H2O+CO2↑;
验证:(1)碳酸钠能与盐酸或硫酸反应生成二氧化碳,所以可取固体加入稀盐酸,有气泡产生说明是碳酸钠;或取样品配制成溶液,滴加和氢氧化钙或氯化钙溶液,若反应生成沉淀,则是碳酸钠,因为氢氧化钠和氢氧化钙或氯化钙不反应;
[拓展应用]碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物;受热可分解生成二氧化碳,故也可作发酵粉;
故答案为:
[探究实验1]药匙;消失(或溶解,合理即可);
[探究实验2]碳酸氢钠溶液呈碱性;
[探究实验3]产生气泡;
[探究实验4]防止水回流使试管破裂;2NaHCO3
Na2CO3+H2O+CO2↑;
验证:取白色固体于试管中,加入稀盐酸,有气泡产生(合理即可);
[拓展应用]治疗胃酸过多(合理均可).
由题意可知:碳酸氢钠是白色粉末,取用粉末状药品用药匙,根据实验结论:碳酸氢钠能溶于水,所以加水后固体会消失、溶解;
【探究实验2】因为碱性溶液能使酚酞变红,所以滴入几滴酚酞试液,振荡.溶液变成红色,说明碳酸氢钠溶液呈碱性;
[探究实验3]
碳酸氢钠和盐酸反应生成二氧化碳气体,所以会看到溶液中能产生气泡;
[探究实验4]
加热碳酸氢钠生成水,所以试管口要低于试管底部,防止水倒流引起试管炸裂;碳酸氢钠充分加热后,大试管壁上有水珠出现,说明生成水,管底有白色固体残留,小试管中澄清石灰石变浑浊,说明生成二氧化碳,据反应前后元素种类不变,可知生成的白色固体是碳酸钠,方程式是:2NaHCO3
| ||
验证:(1)碳酸钠能与盐酸或硫酸反应生成二氧化碳,所以可取固体加入稀盐酸,有气泡产生说明是碳酸钠;或取样品配制成溶液,滴加和氢氧化钙或氯化钙溶液,若反应生成沉淀,则是碳酸钠,因为氢氧化钠和氢氧化钙或氯化钙不反应;
[拓展应用]碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物;受热可分解生成二氧化碳,故也可作发酵粉;
故答案为:
[探究实验1]药匙;消失(或溶解,合理即可);
[探究实验2]碳酸氢钠溶液呈碱性;
[探究实验3]产生气泡;
[探究实验4]防止水回流使试管破裂;2NaHCO3
| ||
验证:取白色固体于试管中,加入稀盐酸,有气泡产生(合理即可);
[拓展应用]治疗胃酸过多(合理均可).
点评:掌握碳酸盐和酸反应放出二氧化碳气体,酚酞试液的变色情况、方程式的书写,以及碳酸钠、氢氧化钠的性质,是解答的基础和关键,该题还较好的考查了学生根据题意分析解决问题、应用知识解决问题的能力.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
下列物质与用途对应关系,不正确的是( )
| A、氧气-供给呼吸 |
| B、烧碱-治疗胃酸过多 |
| C、干冰-人工降雨 |
| D、小苏打-焙制糕点 |
 为验证二氧化碳和氢氧化钠溶液确实能发生化学反应,两个化学兴趣小组的同学进行了如下探究活动.
为验证二氧化碳和氢氧化钠溶液确实能发生化学反应,两个化学兴趣小组的同学进行了如下探究活动.
 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.