题目内容
6.现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末.欲确定R的成分,请你一起完成:(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置.
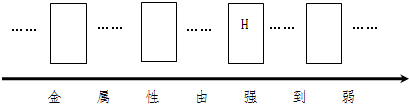
(2)这三种金属中,与盐酸反应最剧烈的是镁(或Mg);取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是银(或Ag).
(3)待不再产生气泡时,再进行过滤(填写一种实验操作方法),得到溶液和铜.然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是铁(或Fe).
(4)写出金属R与稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑.该反应的基本类型属于置换(选填“化合”、“分解”、“置换”或“复分解”)反应.
分析 (1)根据金属活动性顺序,将银、镁、铁三种金属的元素符号填金属活动性顺序表中的相应位置;
(2)根据金属活动性顺序,排在氢前面的金属能和酸反应,后面的金属不能和酸反应分析;
(3)根据操作后得到溶液和铜的结果,判断所进行的实验操作;根据排在前面的金属能把排在后面的金属从它的盐溶液中置换出来分析;
(4)根据对金属R的推断,写出与硫酸反应的化学方程式,并对该反应进行分类.
解答 解:(1)根据银、镁、铁三种金属的活动性强弱关系镁>铁>氢>银,可判断顺序表最左端空格内为镁,接下来的空格内为铁,最右端为银;
(2)这三种金属中,与盐酸反应最剧烈的是镁(或Mg);铜与另一种金属R的混合粉末能与稀硫酸反应放出氢气,可判断金属R能与酸反应产生氢气,由金属R不可能是金属银;
(3)根据操作后把溶液与铜分离开来,可判断该操作为过滤;由于金属和酸反应产生的盐能与锌反应,可判断盐中金属活动性比锌弱,而金属镁的活动性比锌强,因此金属R应为铁;
(4)铁与硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;该反应为单质与化合物生成单质与化合物的置换反应;
故答案为:(1)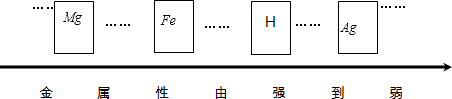
(2)镁(或Mg);银(或Ag);
(3)过滤;铁(或Fe);
(4)Fe+H2SO4=FeSO4+H2↑;置换.
点评 本题属于金属活动性顺序的考查,依据金属活动性顺序中位于氢之前的金属能从酸中置换出氢,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来分析即可.

练习册系列答案
相关题目
16.某物质经分析只含有一种元素,该物质( )
| A. | 一定是单质 | B. | 一定不是单质 | C. | 一定是化合物 | D. | 一定不是化合物 |
15.下列实验方法一定能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 检验一瓶气体是否为CO2 | 将燃着的木条伸入瓶中 |
| B | 鉴别H2和CH4 | 分别点燃,在火焰上方罩一干冷烧杯 |
| C | 除去中CO2的CO | 点燃 |
| D | 鉴别硬水与软水 | 加肥皂水,搅拌 |
| A. | A | B. | B | C. | C | D. | D |
3.氢氧化钠是化学实验室中的常用试剂,盛放NaOH溶液的试剂瓶瓶口常会出现白色粉末.化学兴趣小组的同学对这种白色粉末进行了实验探究.
【提出猜想】他们依据所学的化学知识,对这种白色粉末的成分作了如下三种不同的猜想:
①甲同学认为可能是NaOH; ②乙同学认为可能是Na2CO3;
③丙同学认为可能是NaOH和Na2CO3的混合物.
请将乙同学的猜想填写完整.为了验证猜想,他们进行了下面的实验:
【实验探究】
(1)甲同学取少量白色粉末溶于水,向所得溶液中滴加酚酞溶液,溶液变成红色.由此该同学认为白色粉末是NaOH.请判断他所得出的结论是否正确,并简述理由:不正确,Na2CO3溶液也显碱性,也能使酚酞试液变红色.
(2)乙同学为验证他的猜想,设计了下列实验,请将下列实验报告填写完整.
(3)丙同学认为乙同学得出的结论不严密.为验证自己的猜想,该同学取少量白色粉末溶于水,向所得的溶液中滴加过量的BaCl2溶液,有白色沉淀产生,由此判断白色粉末中含有Na2CO3;该同学继续向溶液中滴加酚酞试液,酚酞试液变红色,证明了自己的猜想正确.
【问题讨论】如果实验室中没有BaCl2溶液,能否用Ba(OH)2溶液代替,并说明理由:不能,Ba(OH)2是碱,对NaOH的鉴定产生干扰.
【提出猜想】他们依据所学的化学知识,对这种白色粉末的成分作了如下三种不同的猜想:
①甲同学认为可能是NaOH; ②乙同学认为可能是Na2CO3;
③丙同学认为可能是NaOH和Na2CO3的混合物.
请将乙同学的猜想填写完整.为了验证猜想,他们进行了下面的实验:
【实验探究】
(1)甲同学取少量白色粉末溶于水,向所得溶液中滴加酚酞溶液,溶液变成红色.由此该同学认为白色粉末是NaOH.请判断他所得出的结论是否正确,并简述理由:不正确,Na2CO3溶液也显碱性,也能使酚酞试液变红色.
(2)乙同学为验证他的猜想,设计了下列实验,请将下列实验报告填写完整.
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| 取少量白色粉末滴加稀盐酸. | 有气泡生成 | 乙同学认为自己的猜想正确.反应的方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O |
【问题讨论】如果实验室中没有BaCl2溶液,能否用Ba(OH)2溶液代替,并说明理由:不能,Ba(OH)2是碱,对NaOH的鉴定产生干扰.
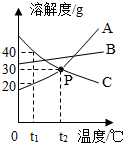 如图是A、B、C三种固体物质的溶解度曲线,它们溶于水时溶液温度均无明显变化.请回答下列问题:
如图是A、B、C三种固体物质的溶解度曲线,它们溶于水时溶液温度均无明显变化.请回答下列问题: 水一命之源
水一命之源