题目内容
11.根据下图回答问题.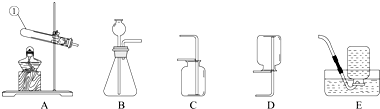
(1)写出仪器①的名称试管.
(2)用高锰酸钾制取氧气应选用的发生装置为A(填字母编号,下同);化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;实验时应在试管口放一团棉花;若改用氯酸钾和二氧化锰来制取氧气,则二氧化锰在反应前后固体混合物中的质量分数将变大(填“变大”、“变小”或“不变”);收集干燥氧气收集装置选C;若某同学用E装置收集一瓶较纯净的氧气,当观察到气泡连续、均匀冒出时开始收集.
(3)实验室制取二氧化碳应选用的装置为B.用大理石和稀盐酸制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到燃着的木条熄灭,说明瓶中已充满二氧化碳.
分析 (1)熟悉常见仪器,了解仪器名称;
(2)根据实验室用高锰酸钾制取氧气需要加热,属于固体加热型选择发生装置,并据反应原理书写方程式,实验时试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管;氯酸钾分解生成氯化钾固体和氧气,二氧化锰是反应的催化剂,反应前后质量不变,收集干燥的气体用排空气法,氧气密度比空气大,反应开始出来的气体中混有空气,据此分析解答;
(3)根据制取二氧化碳用大理石和稀盐酸常温反应属于固液常温型选择发生装置,据反应原理书写方程式,根据二氧化碳不支持燃烧的性质验满.
解答 解:(1)图中编号仪器是试管;
(2)实验室用高锰酸钾制取氧气需要加热,属于固体加热型,故选择发生装置A,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;实验时试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管;氯酸钾分解生成氯化钾固体和氧气,二氧化锰是反应的催化剂,反应前后质量不变,根据质量守恒定律反应后固体混合物的质量减小,所以二氧化锰在反应前后固体混合物中的质量分数将变大;氧气密度比空气大,所以收集干燥的氧气可用向上排空气法,反应开始出来的气体中混有空气,所以要等气泡连续、均匀冒出再开始收集,防止收集的氧气不纯;
(3)制取二氧化碳用大理石和稀盐酸反应生成氯化钙、水和二氧化碳,该反应是固体和液体的不加热反应,所以可选用B作为发生装置,反应的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到木条熄灭,说明收集满了;
故答案为:(1)试管;
(2)A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;一团棉花;变大;C;气泡连续、均匀冒出;
(3)B;CaCO3+2HCl═CaCl2+H2O+CO2↑; 燃着的木条熄灭.
点评 实验室制取氧气和二氧化碳的实验是初中化学重点实验,实验仪器的选择,药品的选择,化学方程式的书写,气体的验满等知识都是经常考查的内容,掌握好基础知识才能灵活运用解答相关问题,发生装置的选择通常依据反应物的状态和反应条件进行选择.

| A. | 11.7g | B. | 5.85g | C. | 10g | D. | 4g |
| A. | 冰水混合物 | B. | 碳酸氢铵 | C. | 钢 | D. | 酒精 |
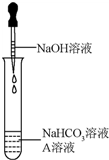 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$NaCO3+H2O+CO2↑
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)实验过程:[实验1]证明反应生成了Na2CO3同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2. 有同学提出这个实验不足以证明有Na2CO3生成,其理由是_CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
[实验2]证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.

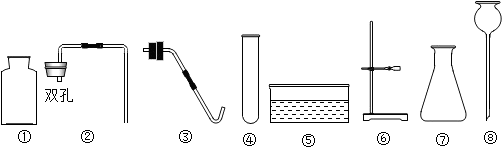
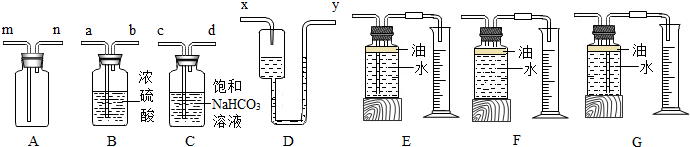
 ,则n的值为17;自来水厂可以采用通氯气方法消毒杀菌,化学方程式为:Cl2+H2O=HClO+HCl.
,则n的值为17;自来水厂可以采用通氯气方法消毒杀菌,化学方程式为:Cl2+H2O=HClO+HCl.